| 結構式 |
|
|
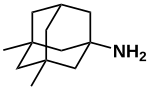
Memantine
1-amino-3,5-dimethyl-adamantane
|
| UpToDate |
UpToDate 連結
|
| 藥理作用 |
|
|
有更多的證據顯示:麩胺酸性神經傳導(glutamatergic neurotransmi-ssion)的官能障礙,尤其在NMDA受器體過度刺激時,會促成神經退化性失智症的症狀表現及疾病進展。Memantine為一電位調控型、中度親和力、非競爭性之NMDA受器拮抗劑,可阻斷因麩胺酸(glutamate) 強度升高作用造成之神經障礙。
|
| 適應症 |
|
|
治療中重度及重度之阿茲海默症。
|
| 用法用量 |
|
第一週為一天一次5mg,之後依醫師處方調整劑量。
1. 若調整為一天10mg,則一天二次各5mg 。
2. 若調整為一天15mg,則早上10mg、晚上5mg。
3. 最大劑量每日20mg。
|
| 藥動力學 |
|
|
吸收:Memantine的生體可用率近乎100%,tmax為3至8小時,食物不會影響memantine的吸收。
線性:從一健康受試者的研究中,已證明於10~40 毫克的劑量範圍內為線性藥物動力學。
分佈:每日Memantine 20 毫克達成之穩定狀態血中濃度範圍為70~150ng/ml (0.5-1 μmol),個體差異很大。當每日劑量為5~30毫克時,平均CSF/serum=0.52,擬似分佈體積約為10 l/kg,約45%的memantine和血漿蛋白結合。
生物轉換:於人體中,80%之memantine相關物質為原型藥物,主要代謝物為N-3,5-dimethyl-gludantan,為4-和6-hydroxy-memantine之異構混合物及1-nitroso-3,5-dimethyl-adamantane。這些代謝物無拮抗NMDA之活性,體外試驗亦無偵測到cytochrome P450催化此代謝反應。一研究指出,口服投與14C-memantine,20天之內可回收84%的藥量, 99%以上則由腎臟排除。
排除:memantine以單指數方式排除,其最終半衰期(terminal half-life)為60~100小時。腎功能正常之受試者,全身清除率(Cl tot)為170 ml/min/1.73m2,部分之總腎臟清除率則來自於腎小管分泌作用。腎功能亦包括腎小管再吸收作用,可能經由陽離子運輸蛋白傳達。於鹼性尿液狀態下,memantine之腎排除率會因pH值升高(7-9)而降低(參考4.4節)。尿液鹼化可能由飲食習慣徹底改變,如肉食者改為素食者,或大量飲用鹼性胃液所導致。
特殊病人族群:在腎功能正常及降低之老年受試者(肌酸酐清除率為50-100 ml/min/1.73m2),觀察到肌酸酐清除率和memantine之總腎臟清率有顯著關聯性(參考4.2節)。肝臟疾病對Memantine之藥物動力學的影響尚未被研究,由於memantine僅少量由肝臟代謝,且其代謝物無拮抗NMDA之活性,因此對於輕微至中度肝臟受損者,並無預期藥物動力學有臨床顯著的改變。
|
| 副作用 |
|
|
幻覺、困惑、暈眩、頭痛、疲倦。
|
| 交互作用 |
|
|
由於memantine的藥理活性和作用機轉,可能發生下列交互作用:
併用NMDA-antagonist如memantine,會增加 L-dopa, dopaminergicagonists, 和anticholinergics的作用,而barbiturates和neuroleptics的作用則被降低。memantine和antispasmodic agents, dantrolene 或baclofen併用,會改變其作用,因此需要調整劑量。
由於藥毒性精神病症的風險,memantine應避免和amantadine併用,兩者的化合物在化學結構上和NMDA-antagonist相關,ketamine和dextromethorphan亦如此。已有一關於memantine和phenytoin併用可能產生危險的案例報告。
其他藥物如cimetidine, ranitidine, procainamide, quinidine, quinine和nicotine使用和amantadine相同的腎陽離子運輸系統(renal cationictransport system) ,亦可能和memantine產生交互作用而導致血中濃度升高的潛在危險。
當memantine 或其他藥物和hydrochlorothiazide(HCT)併用時,可能會降低HCT的排除。Memantine在體外試驗中顯示不會抑制CYP 1A2, 2A6, 2C9, 2D6, 2E1,3A、含monooxygenase之核黃素、epoxide hydrolase和硫酸化的作用。
|
| 禁忌 |
|
|
對Memantine hydrochloride成分過敏者。
|
| 給付規定 |
|
1.3.3.失智症治療藥品
1.限用於依NINDS-ADRDA或DSM或ICD標準診斷為阿滋海默氏症或帕金森氏症之失智症病患。
2.如有腦中風病史,臨床診斷為「血管性失智症」,或有嚴重心臟傳導阻斷(heart block)之病患,不建議使用。
3.初次使用者,需於病歷上記載以下資料:(106/10/1)
(1)CT、MRI或哈金斯氏量表(Hachinski lschemic Score)三項其中之任一結果報告。
(2)CBC, VDRL, BUN, Creatinine, GOT, GPT, T4, TSH檢驗。
(3)MMSE或CDR智能測驗報告。
4.依疾病別及嚴重度,另規定如下:
(1)阿滋海默氏症之失智症由神經科或精神科醫師處方使用。
Ⅰ.輕度至中度失智症:
限使用donepezil、rivastigmine及galantamine 口服製劑(90/10/1、92/1/1、95/6/1、100/3/1、102/8/1、106/10/1):
i.智能測驗結果為MMSE 10~26分或CDR 1級及2級之患者。
ii.使用前述三種藥品任一種後,三個月內,因副作用得換用本類另一種藥物,並於病歷上記載換藥理由。(93/4/1、102/8/1、106/10/1)
iii.使用後每一年需重新評估,追蹤MMSE或CDR智能測驗,並於病歷記錄,如MMSE較前一次治療時減少2分(不含)以上或CDR退步1級,則應停用此類藥品。惟Epalon Tablets、NEPES Tablets、Nomi-Nox Tablets等3種藥品,使用後每一年需重新評估,追蹤MMSE或CDR智能測驗,並於病歷記錄,如MMSE較起步治療時減少2分(不含)以上或CDR退步1級,則應停用此類藥品。(98/1/1、99/5/1、102/8/1、106/10/1)
iv.使用rivastigmine貼片劑(如Exelon Patch),每日限用一片,且不得併用同成分之口服藥品(100/3/1)。
Ⅱ.中重度失智症:
限使用memantine口服製劑(95/6/1、99/10/1、102/8/1、106/10/1)
i. 智能測驗結果為10≦MMSE≦14分或CDR 2級之患者。
ii.曾使用過donepezil, rivastig-mine, galantamine其中任一種藥品之患者,若不再適用上述其中任一藥物,且MMSE或CDR智能測驗達標準(10≦MMSE≦14分或CDR 2級),得換用memantine。惟 memantine 不得與前項三種藥品併用。(106/10/1)
iii.使用後每一年需重新評估,追蹤MMSE或CDR智能測驗,並於病歷記錄,如MMSE較前一次治療時減少2分(不含)以上或CDR退步1級,則應停用此類藥品。惟Ebixa Tablets及Evy Tablets等2種藥品,使用後每一年需重新評估,追蹤MMSE或CDR智能測驗,並於病歷記錄,如MMSE較起步治療時減少2分(不含)以上或CDR退步1級,則應停用此類藥品。(98/1/1、99/5/1、102/8/1、106/10/1)
Ⅲ.重度失智症:(99/10/1、102/8/1)
限使用donepezil及memantine口服製劑 (102/8/1)
i.智能測驗結果為MMSE 5-9分且CDR 3級之患者。
ii.臥床或無行動能力者不得使用。
iii.曾使用過memantine,donepezil, rivastigmine, galantamine而不再適用者,不得使用。
iv.donepezil及memantine二者不能併用。
v.使用後每一年需重新評估,追蹤MMSE智能測驗,如MMSE較前一次治療時減少2分(不含)以上,則應停用此類藥品。惟Epalon Tablets、NEPES Tablets、Nomi-Nox Tablets、Ebixa Tablets 及Evy Tablets等5種藥品,使用後每一年需重新評估,追蹤MMSE智能測驗,如MMSE較起步治療時減少2分(不含)以上,則應停用此類藥品。(99/10/1、102/8/1)
|
| 注意事項 |
|
1.無嚴重腎功能受損病人使用資料(肌酸酐清除率<9 ml/min/1.73 m2),因此不建議使用。
2.應避免和N-methyl-D-aspartate(NMDA)-antagonists如amantadine,ketamine或dextromethorphan併用,這些化合物與memantine作用於相同的受器系統,因此副作用反應(主要和中樞神經相關)可能更為頻繁或強烈。
3.某些因素可能會使尿液酸鹼值上升,需要小心監測病人。這些因素包含飲食習慣徹底改變,如肉食者改為素食者或大量飲用鹼性胃液。此外,腎小管酸中毒(RTA)或由Proteus bacteria引起之嚴重尿道感染也可能導致尿液酸鹼值升高。
|
| 警語 |
|
|
memantine可能改變反應力,應提醒出院病人駕車或操作機械時需特別小心。
|
| 過量處理 |
|
|
病人服用過量之memantine,其作用於中樞神經系統(如:不安、精神異常、視覺上的幻覺、前痙攣proconvulsiveness、嗜睡、木僵、無意識)產生之症狀己被緩解,且無永久性後遺症。服用過量之治療應以緩解症狀為主。
|
| 藥品保存方式 |
|
藥品應置於攝氏 15 ~ 25 度乾燥處所;如發生變質或過期,不可再食用。
|







































