| 結構式 |
|
|
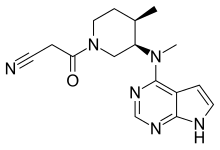
Tofacitinib
(3R,4R)-4-methyl-3-(methyl-7H-pyrrolo [2,3-d]pyrimidin-4-ylamino)-ß-oxo-1-piperidinepropanenitrile, 2-hydroxy-1,2,3-propanetricarboxylate (1:1)。
|
| UpToDate |
UpToDate 連結
|
| 藥理作用 |
|
|
Tofacitinib是一種Janus激酶(JAK)抑制劑。JAKs屬於細胞內酵素,此酵素會將細胞激素或生長因子與接受體在細胞膜上發生交互作用所產生的訊息傳送出去,從而影響造血細胞運轉與免疫細胞功能。在傳遞路徑中,JAKs會促使訊息傳導與轉錄活化因子(STATs)磷酸化及活化,STATs則會調節細胞內的機能,包括基因表現。Tofacitinib可從JAKs這個點來調節此傳遞路徑,並阻止STATs磷酸化與活化。JAK酵素會透過JAKs成對模式(如JAK1/JAK3、JAK1/JAK2、JAK1/TyK2、JAK2/JAK2)傳遞細胞激素所發出的訊息。Tofacitinib可抑制JAK1/JAK2、JAK1/JAK3及JAK2/JAK2等組合體的體外活性,其IC50分別為406、56與1377 nM。不過,目前並不確知特定JAK組合體與治療效果之間的關聯性。
|
| 適應症 |
|
|
1. 類風濕性關節炎
• XELJANZ適用於治療患有中至重度活動性類風濕性關節炎(Rheumatoid Arthritis, RA)且對methotrexate無法產生適當治療反應或無法耐受methotrexate之成人病人。本品可用於單一療法或與methotrexate或其他非生物性的疾病緩解型抗風濕藥物(DMARDs)合併使用。
使用限制:不建議XELJANZ與生物性的疾病緩解型抗風濕藥物(DMARDs),或與強效免疫抑制劑(如azathioprine與cyclosporine)合併使用。
2. 乾癬性關節炎
• XELJANZ與非生物性的疾病緩解型抗風濕藥物(DMARDs)合併使用,適用於治療患有活動性乾癬性關節炎(Psoriatic Arthritis, PsA)且對methotrexate或其他疾病緩解型抗風濕藥物(DMARDs)無法產生適當治療反應或無法耐受之成人病人。
使用限制:不建議XELJANZ與生物性的疾病緩解型抗風濕藥物(DMARDs),或與強效免疫抑制劑(如azathioprine與cyclosporine)合併使用。
3. 僵直性脊椎炎
• 適用於治療曾對非類固醇抗發炎藥物(NSAID)反應不佳或耐受性不良的活動性僵直性脊椎炎(Ankylosing Spondylitis, AS)成人病人。
使用限制:不建議XELJANZ與生物性的疾病緩解型抗風濕藥物(DMARDs),或與強效免疫抑制劑(如azathioprine與cyclosporine)合併使用。
4. 潰瘍性結腸炎
• XELJANZ適用於治療對類固醇、azathioprine、6-mercaptopurine (6-MP)或TNF抑制療法失敗或無法耐受之中度至重度活動性潰瘍性結腸炎成人病人。
使用限制:不建議XELJANZ與治療潰瘍性結腸炎之生物性療法或與強效免疫抑制劑(如azathioprine與cyclosporine)合併使用。
|
| 用法用量 |
|
|
重要使用方法
• 對絕對淋巴球計數低於500細胞/毫米3、絕對嗜中性白血球計數(ANC)低於1000細胞/毫米3或血紅素濃度低於9 g/dL的病人,不可開始使用XELJANZ。
• 建議中斷給藥以處理淋巴球減少、嗜中性白血球減少和貧血的情況。
• 如果病人發生嚴重的感染症,應暫時中斷XELJANZ的治療,直到感染獲得控制。
• XELJANZ為口服給藥,可與食物併服,亦可不與食物併服。
類風濕性關節炎的劑量
本品可用於單一療法或與methotrexate或其他非生物性的疾病緩解型抗風濕藥物(DMARDs)合併使用。XELJANZ的建議劑量為5毫克每日兩次。
乾癬性關節炎的劑量
XELJANZ的建議劑量為5毫克每日兩次,與非生物性的疾病緩解型抗風濕藥物(DMARDs)合併使用。
XELJANZ單一治療的療效還未於乾癬性關節炎進行研究。
僵直性脊椎炎的劑量
XELJANZ的建議劑量為5毫克每日兩次。
潰瘍性結腸炎的劑量
• 誘導劑量為10毫克每日兩次,持續8週。評估病人,並根據治療反應決定是否轉變至維持療法。如有需要,持續10毫克每日兩次治療最多達16週。若仍未達到足夠之治療反應,在誘導治療16週後應停止10毫克每日兩次之治療。
• 維持劑量為5毫克每日兩次。在審慎考量個別病人的效益與風險之下誘導治療後,僅限於對失去治療反應者使用10毫克每日兩次之維持治療,且應盡可能縮短使用10毫克每日兩次的期間。應使用可維持病人治療反應所需之最低有效劑量。
類風溼性關節炎、乾癬性關節炎,與僵直性脊椎炎的建議劑量調整
表1呈現XELJANZ的成人每日建議劑量和接受CYP2C19及/或CYP3A4抑制劑、具有中度或重度腎功能不全(包括但不限於正在接受血液透析的重度功能不全病人)、中度肝功能不全、淋巴球減少、嗜中性白血球減少或貧血病人的劑量調整方式。
|
| 藥動力學 |
|
口服投予XELJANZ之後,會在0.5-1小時內達到尖峰血中濃度,排除半衰期為3小時左右,此外,在治療劑量範圍內,全身曝藥量的升高程度會與劑量成正比。以每日兩次的方式投藥之後,會於24-48小時內達到穩定狀態濃度,且幾無蓄積現象。
吸收
XELJANZ的口服絕對生體可用率為74%。和高脂食物併服後,XELJANZ AUC不會發生改變,但Cmax會降低32%。在臨床試驗中, XELJANZ投與時並未考慮食物的因素[參見劑量與用法(2)]。
分佈
靜脈注射給藥後的分佈體積為87升。Tofacitinib的蛋白質結合率約為40%。Tofacitinib主要都是與白蛋白結合,且似乎並不會與α1酸性醣蛋白結合。Tofacitinib在紅血球與血漿中的分佈情形大致相當。
代謝與排出
Tofacitinib的廓清機制是約70%經由肝臟代謝,30%經由腎臟排泄。Tofacitinib主要經由CYP3A4進行代謝,少部份由CYP2C19負責。一項人類放射性標記研究顯示,循環中的總放射性活性物質,超過65%屬於未改變的tofacitinib,其餘35%則為8種代謝物,各代謝物在總放射性活性物質中所佔的比例都低於8%。Tofacitinib的藥理活性係源自其原形藥物。
|
| 副作用 |
|
|
腹瀉、鼻咽炎、上呼吸道感染、頭痛。
|
| 交互作用 |
|
|
詳見仿單交互作用之內容。
|
| 禁忌 |
|
|
無。
|
| 給付規定 |
|
8.2.4. Tofacitinib(如Xeljanz):(92/3/1、93/8/1、93/9/1、
98/3/1、99/2/1、100/12/1、101/1/1、101/6/1、101/10/1、102/1/1、
102/2/1、102/4/1、102/10/1、103/9/1、103/12/1、105/9/1、105/10/1、
109/12/1)
使用本類藥品之醫事機構應注意監測病患用藥後之不良反應及可能發生的重大
安全事件(如肺結核及病毒性肝炎)。(103/9/1)
8.2.4.2.Tofacitinib(如Xeljanz):(92/3/1、93/8/1、93/9/1、98/3/1、
99/2/1、100/12/1、101/1/1、101/6/1、102/1/1、102/4/1、102/10/1、
103/12/1、106/4/1、106/11/1、107/9/1、108/3/1、108/5/1、109/8/1、
109/9/1、109/12/1、110/3/1、110/5/1、110/6/1):成人治療部分
因篇幅關係詳見健保局之藥品給付規定相關章節
8.2.4.3. Tofacitinib (如Xeljanz) (98/8/1、98/11/1、101/1/1、102/1/1、107/1/1、109/9/1、109/12/1、110/7/1、111/5/1、112/3/1、112/4/1):用於僵直性脊椎炎治療部分
因篇幅關係詳見健保局之藥品給付規定相關章節
8.2.4.4.Tofacitinib (如Xeljanz):(98/8/1、98/11/1、99/1/1、102/1/1、102/2/1、
105/10/1、107/1/1、109/3/1、109/6/1、109/8/1、109/9/1、110/7/1)
(98/8/1、98/11/1、99/1/1、102/1/1、102/2/1、105/10/1、107/1/1、
109/3/1、109/6/1、109/8/1、109/9/1、110/7/1、111/3/1):用於活動性乾癬性
關節炎-乾癬性周邊關節炎治療部分
因篇幅關係詳見健保局之藥品給付規定相關章節
8.2.4.5.Tofacitinib (如 Xeljanz) (98/8/1、98/11/1、
99/1/1、102/1/1、102/2/1、107/1/1、109/3/1、109/6/1、110/7/1):用於活
動性乾癬性關節炎-乾癬性脊椎病變治療部分
因篇幅關係詳見健保局之藥品給付規定相關章節
8.2.4.9.Golimumab(如Simponi)、Adalimumab(如Humira)、Vedolizumab (如Entyvio)、infliximab(如Remicade)、tofacitinib(如Xeljanz)(105/9/1、105/10/1、106/10/1、107/8/1、108/10/1、111/3/1、111/6/1):用於潰瘍性結腸炎治療部分
因篇幅關係詳見健保局之藥品給付規定相關章節
8.2.4.9.1.Tofacitinib(如Xeljanz) (105/9/1、105/10/1、106/10/1、107/8/1、108/10/1、111/3/1、111/6/1):成人治療部分
因篇幅關係詳見健保局之藥品給付規定相關章節
|
| 警語 |
|
嚴重感染
病人使用XELJANZ治療時,發生可能導致住院或死亡之嚴重感染症的風險會升高、不良反應]。發生這些感染症的病人大部份都曾同時使用免疫抑制劑(如methotrexate)或皮質類固醇。
如果發生嚴重的感染症,應暫時停用XELJANZ,直到感染獲得控制。
死亡
在一項大型、進行中的上市後安全性試驗中,50歲(含)以上,合併至少1項心血管(CV)風險因子的類風濕性關節炎病人接受XELJANZ 10毫克每日兩次治療時,相較於接受XELJANZ 5毫克每日兩次或TNF阻斷劑治療者,有較高的總死亡率,包括心血管猝死。
惡性腫瘤
在使用XELJANZ治療的病人中,曾觀察到發生淋巴瘤與其它惡性腫瘤的病例。在接受XELJANZ治療並同時使用免疫抑制藥物的腎臟移植病人中,曾觀察到Epstein Barr病毒相關性移植後淋巴增生疾病的發生率升高的現象。
血栓
接受XELJANZ和其他Janus激酶抑制劑(用於治療發炎性疾病) 的病人曾發生血栓,包括肺栓塞、深層靜脈血栓以及動脈血栓。在一項大型、進行中的上市後安全性試驗中,50歲(含)以上,合併至少1項心血管風險因子的類風濕性關節炎病人接受XELJANZ 10毫克每日兩次治療時,相較於接受XELJANZ 5毫克每日兩次或TNF阻斷劑治療者,觀察到這些事件的發生率增加。其中有許多嚴重事件,某些事件甚至導致死亡。應避免對有風險病人使用XELJANZ,讓出現血栓症狀的病人停用XELJANZ,並立刻進行評估。
針對潰瘍性結腸炎病人,使用達到/維持治療反應所需的XELJANZ最低有效劑量與最短治療時間。
|
| 過量處理 |
|
對健康志願者投予最高達(包括)單劑100毫克之劑量的藥物動力學資料顯示,預期有超過95%的投予劑量會在24小時內排出體外。
XELJANZ過量並無任何特定的解毒劑。如果用藥過量時,建議應監測患者是否出現不良反應的徵兆與症狀。發生不良反應的患者應接受適當的治療。
|
| 藥品保存方式 |
|
|
儲存於 30℃以下。
|







































