| 結構式 |
|
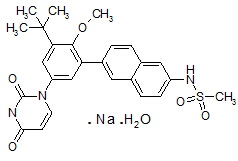
Dasabuvir
N-{6-[5-(2,4-Dioxo-3,4-dihydro-1(2H)-pyrimidinyl)-2-methoxy-3-(2-methyl-2-propanyl)phenyl]-2-naphthyl}methanesulfonamide
|
| UpToDate |
UpToDate 連結
|
| 藥理作用 |
|
Dasabuvir 是由NS5B 基因編碼的HCV RNA 依賴RNA 聚合酉每的非核 抑制劑,而NS5B 基因則對於病毒基因體複製非常重要。
將dasabuvir 與ombitasvir/paritaprevir/ritonavir 併用作用機制不同且抗藥性概況未重複的三種直接抗病毒藥物,針對HCV 病毒生命週期的多個步驟進行治療。
|
| 適應症 |
|
|
Exviera適用於與Viekirax、ribavirin併用,以治療成人慢性C型肝炎基因型1之感染。
|
| 用法用量 |
|
|
建議口服劑量為兩錠Viekirax 12.5/75/50mg 錠劑,每日一次(早上), 以及一錠Exviera 250mg錠劑,每日兩次(早上與晚上)。
|
| 藥動力學 |
|
吸收
Dasabuvir 口服吸收後的平均Tmax 約為4 至5 小時。 Dasabuvir 的曝藥量隨著劑量呈現比例性的增加,累積極低。 與ombitasvir/paritaprevir/ritonavir 併用時, dasabuvir 在給藥約12 日後達到藥動學穩定態。
分布
Dasabuvir 會高度與血漿蛋白質結合。 腎功能或肝功能不全病患的血漿蛋白質結合並未表現出有意義的改變。
人體的血液與血漿濃度比範圍為0.5 至0.7, 顯示dasabuvir 大多分布於全血的血漿部分。 Dasabuvir 在濃度範圍介於0.05 至5 �g/mL 時有超過99.5% 與人類血漿蛋白結合, dasabuvir 的M1 主要代謝物則有94.5%。
生物轉化
Dasabuvir 主要由CYP2C8 代謝, 而較少部分由CYP3A 代謝。 人體在接受14C-dasabuvir 400 mg 劑量後,血漿中的藥物相關放射線活性主要成分( 約60% ) 為原型dasabuvir。 血漿中共找出7 種代謝物。 數量最多的血漿代謝物為M1, 給予單一劑量後, 約佔血液循環中21% 的藥物相關放射線活性(AUC);其主要由CYP2C8
經氧化代謝合成。
排除
在給予dasabuvir 合併ombitasvir/paritaprevir/ritonavir 後, dasabuvir 的平均血漿半衰期約為6 小時。 給予14C-ombitasvir 400mg後, 約有94% 的放射線活性出現於糞便中, 而尿液的放射線活性有限(2%)。
|
| 副作用 |
|
|
疲倦與噁心。
|
| 禁忌 |
|
1. 已知會對活性成分或對任何賦形劑產生過敏反應。
2. 由於潛在的毒性風險, 禁用於中度至重度肝功能不全的病患(Child-Pugh B 與 C) 。
3. 使用含ethinylestradiol 的藥品, 例如大部分複方口服避孕藥或避孕陰道環的藥物成分。
4. Exviera 與強效或中效酵素誘導劑藥品併用預計會降低dasabuvir 的血漿濃度並降低其療效。
|
| 給付規定 |
|
10.7.6.Ombitasvir/paritaprevir/ritonavir(如Viekirax)及dasabuvir (如Exviera) (106/1/24、106/5/15、107/6/1):
1.限用於參加「全民健康保險加強慢性B型及C型肝炎治療計畫」之成人慢性病毒性C型肝炎患者。
2.Ombitasvir/paritaprevir/ ritonavir與dasabuvir合併使用於Anti-HCV陽性超過六個月(或HCV RNA陽性超過六個月)、HCV RNA為陽性、無肝功能代償不全之病毒基因型第1型成人病患,且需符合下列條件:(106/5/15、107/6/1)
經由肝組織切片或肝臟纖維化掃描或FIB-4證實,等同METAVIR system纖維化大於或等於F3;或超音波診斷為肝硬化併食道或胃靜脈曲張,或超音波診斷為肝硬化併脾腫大。
註:以肝臟纖維化掃描或Fibrosis-4 (FIB-4)證實等同METAVIR system纖維化大於或等於F3之定義為:
Ⅰ.肝臟纖維化掃描transient elastography (Fibroscan)≧9.5Kpa或Acoustic Radiation Force Impulse elastography (ARFI)≧1.81m/sec。
Ⅱ.Fibrosis-4 (FIB-4)≧3.25,計算公式為[Age(years) × AST(U/L)] / [Platelet count(109/L) × √ALT(U/L)]。
3.給付療程如下,醫師每次開藥以4週為限。服藥後需定期監測病毒量,使用4週後病毒量未能下降超過二個對數值(即下降未達100倍)者,應停止治療,給付不超過6週。
(1)基因型1a型且無肝硬化者,需合併ribavirin治療,給付12週。
(2)基因型1a型且具代償性肝硬化(Child-Pugh score A)者,需合併ribavirin治療,給付24週。
(3)基因型1b型且無肝硬化者或具代償性肝硬化(Child-Pugh score A)者,給付12週。
4.限未曾申請給付其他同類全口服直接抗病毒藥物(direct-acting anti-viral, DAAs),且不得併用其他DAAs。
|
| 注意事項 |
|
|
一般Exviera 不建議做為單一藥物治療, 必須併用其他藥品治療C 型肝炎感染。
|
| 過量處理 |
|
|
若發生用藥過量, 建議應監測該名病患是否出現不良反應或不良影響的任何徵兆或症狀, 並應立即施予適當的症狀性治療。
|
| 藥品保存方式 |
|
|
儲存於30°C以下。
|







































