| 結構式 |
|
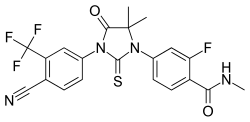
Enzalutamide
|
| UpToDate |
UpToDate 連結
|
| 藥理作用 |
|
|
已知前列腺癌對雄性素敏感,並對抑制雄性素受體訊息傳遞有反應。儘管血清中雄性 素濃度低,甚至檢測不到,雄性素受體訊息傳遞仍持續促使疾病惡化。經由雄性素受 體刺激腫瘤細胞生長需要入核活化及 DNA 結合。Enzalutamide 是強效雄性素受體訊息 傳遞抑制劑,阻斷雄性素受體訊息傳遞路徑的幾個步驟。Enzalutamide 競爭性抑制雄性素與雄性素受體的結合,抑制被活化受體入核(nuclear translocation),並抑制被活化雄 性素受體與 DNA 結合,即使在雄性素受體過度表現與對抗雄性素有抗藥性的前列腺癌 細胞情況下也是一樣。Enzalutamide 的治療減低前列腺癌細胞的生長,並能誘導癌細胞 死亡和腫瘤萎縮。在臨床前研究,enzalutamide 沒有雄性素受體作用活性。
|
| 適應症 |
|
治療
(1)藥物或手術去勢抗性的轉移性前列腺癌,且在雄性素去除療法失敗後屬無症狀或輕度症狀而不須使用化學治療者。
(2)藥物或手術去勢抗性的轉移性前列腺癌且已接受過 docetaxel 治療者。
|
| 用法用量 |
|
建議劑量為口服 enzalutamide 160mg (4 粒 40mg 膠囊)每天一次。 對非手術去勢的病患,應持續以 LHRH 類似物做藥物去勢治療。
Xtandi 口服使用。膠囊應以水整粒吞服,可隨餐或空腹服用。
|
| 藥動力學 |
|
吸收
Enzalutamide 的最高血漿濃度(Cmax)於患者服藥後 1-2 小時觀察到。根據在人類進行的質量平衡研究,預測 enzalutamide 的口服吸收至少是 84.2%。Enzalutamide 不是外排運輸蛋白 P-gp 或 BCRP 的受質。在穩定狀態下,enzalutamide 及其活性代謝物的平均Cmax 值分別是 16.6 μg/mL (變異係數[CV] 23%)及 12.7 μg/mL (30% CV)。
分佈
患者口服單一劑量後,enzalutamide 的平均擬似分佈體積(V/F)是 110 L (29% CV)。
Enzalutamide 有 97%至 98%與血漿蛋白結合,主要是白蛋白。活性代謝物有 95%與血漿蛋白結合。
生物轉化
Enzalutamide 被廣泛代謝。人類血漿中有兩種主要代謝物:N-desmethyl enzalutamide(活性)和 carboxylic acid 衍生物(無活性)。Enzalutamide 主要被 CYP2C8 代謝,少部分被CYP3A4/5 代謝,這兩者在活性代謝物形成上扮演某種角色。
排除
Enzalutamide 在患者的平均擬似清除率(CL/F)範圍從 0.520 到 0.564 L/h。
|
| 副作用 |
|
|
最常見的不良反應為無力/疲勞、熱潮紅、頭痛和高血壓。
|
| 交互作用 |
|
其他藥物影響 enzalutamide 曝露量的可能性
CYP2C8 抑制劑和誘導劑
在 enzalutamide 治療期間應避免或小心使用CYP2C8 的強效抑制劑(如 gemfibrozil)或誘導劑(如 rifampicin)。如果患者必須併用強效CYP2C8 抑制劑,enzalutamide 的劑量應降至 80mg 每天一次。
CYP3A4 抑制劑和誘導劑
CYP3A4 在 enzalutamide 的代謝扮演次要的角色。給予健康男性受試者口服強效CYP3A4 抑制劑 itraconazole (200 mg 每天一次)後,enzalutamide 的 AUC 增加 41%,而Cmax 無變化。至於未結合的 enzalutamide 加上未結合的活性代謝物的總和,AUC 增加
27%,而 Cmax 仍無變化。因此,Xtandi 與 CYP3A4 的抑制劑或誘導劑併用時,無須調整劑量。
Enzalutamide 影響其他藥物曝露量的可能性
酵素誘導
Enzalutamide 是強的酵素誘導劑,並且增加許多酵素和運輸蛋白的合成;因此,預測會與許多屬於酵素或運輸蛋白受質的藥物產生交互作用。血漿濃度可能大幅下降,以致喪失或減低臨床效果。也有增加活性代謝物形成的風險。
|
| 禁忌 |
|
1.對活性成份或賦形劑清單中所列任一賦形劑過敏。
2.孕婦或可能懷孕的婦女。
|
| 給付規定 |
|
9.54.Enzalutamide(如Xtandi):(105/9/1、106/9/1、108/3/1、109/10/1、110/3/1、110/11/1、111/3/1、112/9/1)
1.治療高風險非轉移性去勢抗性前列腺癌(high risk nmCRPC)的成年男性。(112/9/1)
(1)須經事前審查核准後使用。
(2)初次申請時需檢附病理報告、使用雄性素去除療法紀錄,系列PSA和睪固酮數據,三個月內影像報告證明無遠端轉移。
(3)ECOG分數須≦1。
(4)PSA doubling time≦10個月,PSA倍增之時間,應依線性回歸模型計算,且其參數取得需基於下列原則:
Ⅰ.至少三個連續PSA測量值,且各測量值皆≧0.2 ng/mL(最高的PSA值必須>1.0ng/ml)。
Ⅱ.應包含先前ADT治療期間的測量值,且最少一測量值為最近3個月內測得之PSA數值。
Ⅲ.第一個和最後一個PSA測量值間隔需≧8週,但≦12個月。
(5)每3個月需再次申請,申請之療程以3個月為限。再次申請時,有 PSA progression 者,需檢附影像學報告,若影像學報告證實轉移,則需停藥;無PSA progression 者,則每6個月需檢附影像學報告,若影像學報告證實轉移,則需停藥。
註:
PSA progression 定義為:PSA下降達最低值(nadir)後,出現 PSA 值上升較 nadir≧25%,且PSA≧2 ng/mL,並於至少3週後,再次抽血確認PSA值有上升趨勢。
2.治療高風險轉移性的去勢敏感性前列腺癌(mCSPC),且與雄性素去除療法併用,總療程以24個月為上限。高風險需符合下列三項條件中至少兩項(限Xtandi):(111/3/1)
(1)葛里森分數(Gleason score)≧8。
(2)骨骼掃描出現三個(含)以上病灶且至少其中一處以上為非中軸骨及骨盆腔轉移。
(3)出現內臟轉移。
3.治療藥物或手術去勢抗性的轉移性前列腺癌(mCRPC),且在雄性素去除療法失敗後屬無症狀或輕度症狀(ECOG分數0或1),未曾接受化學治療者:(106/9/1)
(1)若病患先前接受雄性素去除療法時,在小於12個月的時間內演化成去勢抗性前列腺癌(CRPC),且葛里森分數(Gleason score)≧8時,不得於使用化學治療前使用enzalutamide。(106/9/1)
(2)申請時需另檢附:(106/9/1)
I.用藥紀錄(證明未常規使用止痛藥物,屬無症狀或輕度症狀)。
II.三個月內影像報告證明無臟器轉移。
4.治療藥物或手術去勢抗性的轉移性前列腺癌(ECOG分數須≦2)且已使用過docetaxel 2個療程以上治療無效者。
5.前述2、3、4項經事前審查核准後使用,每3個月需再次申請。(111/3/1、112/9/1)
(1)申請時需檢附病理報告、使用雄性素去除療法紀錄及系列PSA和睪固酮數據。(106/9/1)
(2)再申請時若PSA值下降未超過治療前的50%以上,則需停藥。(106/9/1、109/10/1)
(3)下降達最低值後之持續追蹤出現PSA較最低值上升50%以上且PSA≧2ng/ml,則需停藥,但影像學證據尚無疾病進展者,可以繼續使用。(106/9/1、109/10/1)
6.去勢抗性前列腺癌(CRPC)病患若於化學治療前先使用過enzalutamide,當化學治療失敗後不得再申請使用enzalutamide。(106/9/1)
7.不論病人處於轉移或非轉移的狀態下,終生僅能接受一種治療前列腺癌的新型荷爾蒙藥品(abiraterone、apalutamide、darolutamide和enzalutamide) 且僅能擇一給付,無效後不再給付其他新型荷爾蒙藥品,且除非出現嚴重不耐受反應導致必須永久停止治療的情況,不得互換。(112/9/1)
8.本品與radium-223 dichloride不得合併使用。(108/3/1)
|
| 飲食提示 |
|
|
食物對於 enzalutamide 的曝露程度沒有臨床顯著影響。在臨床試驗中,Xtandi 的給藥無需考慮食物的影響。
|
| 警語 |
|
Enzalutamide 可能對駕駛和操作機器能力有中度影響,因為曾有精神和神經事件,包括痙攣發作的報告。
有痙攣病史或其他誘發因子的患者應被告知駕駛或操作機器的危險性。沒有研究確定 enzalutamide 對駕駛和操作機器能力的影響。
|
| 過量處理 |
|
|
沒有 enzalutamide 的解毒劑。發生藥物過量時,應停止 enzalutamide 的治療,考量半衰期 5.8 天,開始實施一般支持性措施。藥物過量後,患者痙攣發作的風險可能提高。
|
| 藥品保存方式 |
|
|
25℃以下儲存。
|







































