| 結構式 |
|
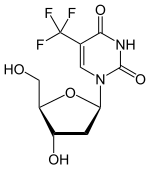
Trifluridine
5-chloro-6-[(2-iminopyrrolidin-1-yl)methyl]pyrimidine-2,4-(1H ,3H )-dione monohydrochloride 或2,4(1H ,3H )-Pyrimidinedione, 5-chloro-6-([ 2-imino-1-pyrrolidinyl)methyl]-, hydrochloride(1:1)
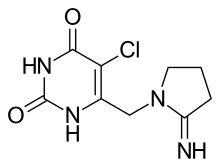
Tipiracil
|
| UpToDate |
UpToDate 連結
|
| 藥理作用 |
|
朗斯弗是由胸腺嘧啶基底的核苷類似物trifluridine,及thymidine phosphorylase 抑制劑tipiracil, 以莫耳數比1:0.5( 重量比為1:0.471) 所組成。內含的tipiracil 可抑制trifluridine 被thymidine phosphorylase 代謝而增加trifluridine 的暴露。
Trifluridine 進入癌細胞後,會嵌入DNA 並干擾DNA 合成及抑制細胞增生。證實Trifluridine/tipiracil 對小鼠身上的KRAS 野生型及突變型人類大腸直腸腫瘤移植具抗腫瘤活性。
|
| 適應症 |
|
|
朗斯弗適用於治療先前曾接受下列療法的轉移性大腸直腸癌之成人患者,包括 fluoropyrimidine、oxaliplatin 及 irinotecan 為基礎的化療,和抗血管內皮生長因子(anti-VEGF)療法;若 RAS 為原生型(wild type),則需接受過抗表皮生長因子受體(anti-EGFR)療法。
|
| 用法用量 |
|
|
朗斯弗的初始建議劑量為每劑 35 毫克 / 平方公尺,至多每劑 80 毫克(劑量以 trifluridine 之含量表示),每日兩次,早晚餐後一小時內服用。一個週期為 28 天,於第 1 天至第 5 天及第 8 天至第 12 天服藥,直到疾病惡化或是發生無法耐受之副作用;劑量的計算為進位至最接近之5 的倍數。
|
| 藥動力學 |
|
吸收
在癌症病患口服一劑35 毫克/ 平方公尺的朗斯弗後, 其
trifluridine 達到最高血中濃度的時間(Tmax)平均約為2小時。
分布
Trifluridine 大部分結合至人類血漿白蛋白。Trifluridine 在人
類血漿的生體外蛋白結合超過96%,不受藥物濃度及tipiracil
的存在影響。Tipiracil 的血漿蛋白結合低於8%。
排除
代謝
Trifluridine 及tipiracil 不會被細胞色素P450(CYP)酶代謝。
Trifluridine 主要經由thymidine phosphorylase 代謝排除,
形成無活性代謝物5-(trifluoromethyl)uracil(FTY)。沒有
其他主要代謝物在血漿或尿液中被檢測出來。
排泄
口服一劑朗斯弗(60 毫克)和[14C]-trifluridine 後,總累積
排出的放射活性為投與劑量的60%。大部分回收的放射活性,是24 小時內經尿液(55 %)排除的FTY 和trifluridine glucuronide 異構物,而糞便與呼氣兩者的排出小於3%。在尿液與糞便中回收到的原型trifluridine 低於投與劑量的3%。
口服一劑朗斯弗(60 毫克)和[14C]-tipiracil hydrochloride 後,回收的放射活性為劑量的77%,包含27% 尿液排出與50% 糞
便排出。在尿液和糞便中,tipiracil 為主要成份,6-HMU 為主
要代謝物。
|
| 副作用 |
|
|
貧血、嗜中性白血球低下、無力 / 疲倦、噁心、血小板低下、食慾減退、腹瀉、嘔吐、腹痛及發燒。
|
| 交互作用 |
|
Trifluridine 是thymidine phosphorylase 的受質,且不會被
細胞色素P450(CYP)酶代謝。Tipiracil 不會被人類肝臟或
肝細胞代謝。
體外研究指出,trifluridine、tipiracil 及FTY 不會抑制CYP
酶,且對於CYP1A2、CYP2B6 及CYP3A4/5 不具誘導作用。
體外研究指出,trifluridine 並非人類攝取及外排轉運蛋白
(uptake and efflux transporters)的抑制劑或受質。
|
| 禁忌 |
|
|
無。
|
| 給付規定 |
|
9.66.Trifluridine/tipiracil(如Lonsurf):(107/12/1、109/12/1、110/6/1)
1.轉移性大腸直腸癌:
(1)用於治療先前曾接受下列療法的轉移性大腸直腸癌之成人患者,包括fluoropyrimidine, oxaliplatin及irinotecan為基礎的化療,和抗血管內皮生長因子(anti-VEGF)等療法;若RAS為原生型(wild type),則需再加上接受過抗表皮生長因子受體(anti-EGFR)療法。(110/6/1)
(2)須經事前審查核准後使用,每次申請事前審查之療程以8週為限,再次申請必須提出客觀證據(如:影像學)證實無惡化,才可繼續使用。
(3)本藥品不得與regorafenib併用。
2.轉移性胃癌:(109/12/1)
(1)用於治療先前曾接受兩種(含)以上治療(包括含fluoropyrimidine–、platinum–、taxane–或 irinotecan為基礎的化學療法,以及HER2/neu標靶治療[如果適合])的轉移性胃腺癌或胃食道接合處腺癌病人。
(2)須經事前審查核准後使用,每次申請事前審查之療程以8週為限,再次申請必須提出客觀證據(如:影像學)證實無惡化,才可繼續使用。
|
| 注意事項 |
|
|
應告知懷孕婦女對於胎兒的潛在風險,提醒具生育能力的女性在朗斯弗治療期間採取有效的避孕措施。
|
| 警語 |
|
嚴重骨髓抑制
在臨床試驗1 中,朗斯弗引起嚴重且危及生命的骨髓抑制(第
3-4 級),包括有貧血(18%)、嗜中性白血球低下(38%)、血小
板低下(5%)以及嗜中性白血球低下發燒(3.8%)等。一位病患
(0.2%)因嗜中性白血球低下合併感染而死亡。在臨床試驗1 中,
接受朗斯弗治療的病患中有9.4% 的病患使用顆粒球聚落刺激因子
(granulocyte-colony stimulating factors)。
每個週期前與第15 天測量全血球數,且可依臨床指示更頻繁地測
量。有嗜中性白血球低下發燒、第4 級嗜中性白血球低下或血小
板數小於50,000/ 立方毫米時,應暫停使用朗斯弗。當恢復時,合
乎條件者,以調降的劑量重新開始朗斯弗治療。
|
| 過量處理 |
|
臨床試驗中給予朗斯弗的最高劑量是每天180 毫克/ 平方公尺。
並無已知的解毒劑可用於朗斯弗藥物過量。
|
| 藥品保存方式 |
|
|
儲存於25℃以下。
|







































