| 結構式 |
|
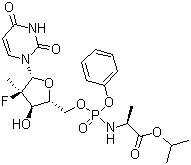
Sofosbuvir
Isopropil (2S)-2-[[[(2R,3R,4R,5R)-5-(2,4-diossopirimidin-1-il)-4-fluoro-3-idrossi-4-metil-tetraidrofuran-2-il]metossi-fenossi-fosforil]amino]propanoato

Velpatasvir
|
| UpToDate |
UpToDate 連結
|
| 藥理作用 |
|
Sofosbuvir 為HCV NS5B RNA 依賴性RNA 聚合酶的泛基因型抑制劑,此聚合酶乃是病毒複製所必需的酵素。Sofosbuvir 是一種核苷酸前驅藥,此前驅藥會經由細胞內代謝作用形成具藥理活性的尿苷酸類似物三磷酸鹽(GS-461203),然後可透過NS5B 聚合酶的作用嵌入HCV RNA,從而產生鏈終止的作用。GS-461203
(sofosbuvir 的活性代謝物)並非人類DNA 與RNA 聚合酶的抑制劑,也不是粒線體RNA聚合酶的抑制劑。
Velpatasvir 為針對HCV NS5A蛋白產生作用的HCV抑制劑,此蛋白乃是RNA複製與組成病毒粒子所必需的物質。體外抗藥性選擇與交叉抗藥性研究顯示,velpatasvir會針對NS5A產生作用,這也是其作用模式。
|
| 適應症 |
|
|
Epclusa 適用於治療成人的慢性C型肝炎病毒(HCV)基因型1、2、3、4、5 或6 之感染症。
|
| 用法用量 |
|
1. Epclusa 的建議劑量為每日一次隨食物或不隨食物口服一錠。 2. 未曾接受治療與曾經接受治療,未併有肝硬化的患者及併有代償性肝硬化的患者,療法與療程為使用Epclusa 治療12 週。
3. 未曾接受治療與曾經接受治療,併有失代償性肝硬化的患者,療法與療程為使用Epclusa + ribavirinb 治療12 週。
4. 由於本品帶有苦味,因此建議不要將膜衣錠嚼碎或研碎使用。 5. 應囑咐患者,如果在服藥後3 小時內發生嘔吐,應另外服用一錠Epclusa。如果在服藥超過3小時之後發生嘔吐,則不須另外再服一劑Epclusa。
6. 如果漏服一劑Epclusa,但仍在正常服藥時間的18小時之內,應指示患者儘快服用該錠藥物,然後患者應於平常的時間服用下一劑藥物。如果已經超過18 小時,則應指示患者繼續等候,然後於平常的時間服用下一劑Epclusa。應囑咐患者切勿一次服用兩倍劑量的Epclusa。
|
| 藥動力學 |
|
|
吸收
曾針對健康成人受試者與慢性C 型肝炎患者評估sofosbuvi r、GS-331007 及velpatasvir 的藥物動力學特性。口服投予Epclusa 之後,sofosbuvir 會快速被吸收進入體內,並可於投藥後1 小時觀察到尖峰中位血中濃度。投藥後3 小時可觀察到GS-331007 的中位尖峰血中濃度。投藥後3 小時可觀察到velpatasvir 的中位尖峰血中濃度。
分佈
Sofosbuvir 與人類血漿蛋白的結合率約為61-65%,且在1 微克/ 毫升至20 微克/ 毫升的範圍內,此結合作用並不會受到藥物濃度的影響。GS-331007 在人類血漿中的蛋白結合率極低。對健康受試者投予單劑400 毫克的[14C]-sofosbuvir 之後,[14C] 放射活性的血液血漿比約為0.7。
Velpatasvir 與人類血漿蛋白的結合率約為> 99.5%,且在0.09 微克/ 毫升至1.8 微克/毫升的範圍內,此結合作用並不會受到藥物濃度的影響。對健康受試者投予單劑100毫克的[14C]-velpatasvir 之後,[14C] 放射活性的血液血漿比介於0.52 與0.67 之間。
生物轉化
Sofosbuvir 會在肝臟進行廣泛的代謝,形成具藥理活性的核苷類似物三磷酸鹽GS-461203。
Velpatasvir 是CYP2B6、CYP2C8 與CYP3A4 的作用受質,但轉化速度緩慢。投予單劑100 毫克的[14C]-velpatasvir 之後,血漿中的放射活性成分大部份(> 98%)為原形母藥。在人類血漿中檢出的代謝物為單羥化及去甲基化的velpatasvir。未改變的velpatasvir 是出現於糞便中的主要成分。
排除
口服單劑400 毫克的[14C]-sofosbuvir 之後,[14C] 放射活性的平均總回收量大於92%,其中分別約有80%、14%與2.5%是自尿液、糞便與呼氣中回收而得。自尿液回收的sofosbuvir 劑量大部份為GS-331007(78%),另有3.5%為sofosbuvir。
這些資料顯示,腎臟廓清是GS-331007 的主要排除途徑。投予Epclusa 之後,sofosbuvir 與GS-331007 的終端半衰期中位數分別為0.5 與25 小時。
口服單劑100 毫克的[14C]-velpatasvir 之後,[14C] 放射活性的平均總回收量為95%,其中分別約有94%與0.4%是自糞便與尿液中回收而得。未改變的velpatasvir 是出現於糞便中的主要成分,平均相當於投予劑量的77%,其次為單羥化velpatasvir(5.9%)與去甲基化velpatasvir( 3.0%)。這些資料顯示,母藥透過膽汁排泄是
velpatasvir 的主要排除途徑。投予Epclusa 之後,velpatasvir 的終端半衰期中位數約為15 小時。
|
| 副作用 |
|
|
頭痛、疲倦及噁心。
|
| 交互作用 |
|
Epclusa 對其他藥物造成影響的可能性
Velpatasvir 乃是藥物運輸蛋白P-gp、乳癌抗藥蛋白(BCRP)、有機陰離子運輸多肽(OATP) 1B1 及OATP1B3 的抑制劑。將Epclusa 與屬於這些運輸蛋白之作用受質的藥物併用可能會升高這些藥物的暴露量。與P-gp( digoxin)、BCRP( rosuvastatin)
及OATP( pravastatin)之敏感受質的交互作用請參見仿單中表2。
|
| 禁忌 |
|
|
對活性成分或所列之任何賦形劑過敏。
|
| 給付規定 |
|
10.7.11. Sofosbuvir/velpatasvir(如 Epclusa)(108/6/1、109/1/1、109/7/1、110/6/1、112/5/1)
1.限用於慢性病毒性 C 型肝炎患者,並依據「C 型肝炎全口服新藥健保給付執行計畫」辦理。(109/1/1、109/7/1、112/5/1)
2.限使用於 HCV RNA 為陽性之病毒基因型第 1 型、第 2 型、第 3 型、第 4 型、第 5 型或第 6 型12歲以上且體重至少30公斤之兒童與成人病患。(112/5/1)
3.給付療程如下,醫師每次開藥以 4 週為限。(110/6/1、112/5/1)
(1)未曾接受全口服直接抗病毒藥物(direct-acting anti-viral, DAAs)或曾接受DAAs治療,未併有或併有代償性肝硬化(Child-Pugh score A)者,給付12週。
(2)未曾接受DAAs或曾接受DAAs治療(含NS5A抑制劑之DAAs治療失敗者除外),併有失代償性肝硬化(Child-Pugh score B或C)者,需合併ribavirin治療,給付12週。(112/5/1)
(3)曾接受含NS5A抑制劑之DAAs治療失敗,併有失代償性肝硬化(Child-Pugh score B或C)者,需合併ribavirin治療,給付24週。(112/5/1)
4.限未曾申請給付其他同類全口服直接抗病毒藥物 (direct- acting anti-viral,DAAs),且不得併用其他 DAAs ,惟若符合下列情形之一者,可再治療一次(一個療程):(110/6/1、112/5/1)。
(1)接受本項藥品或其他DAAs第一次治療時中斷療程,且中斷原因屬專業醫療評估必須停藥者。
(2)接受本項藥品或其他DAAs第一次治療結束後第12週,血中偵測不到病毒,目前血中又再次偵測到病毒者。
(3)接受未含NS5A抑制劑之DAAs第一次治療,於治療完成時或治療結束後第12週,血中仍偵測到病毒者,或治療4週後之病毒量未能下降超過二個對數值(即下降未達100倍)發生在108年1月1日前者。
(4)失代償性肝硬化(Child-Pugh B或C)病患,先前接受含NS5A 抑制劑之DAAs第一次治療失敗者(治療完成時或治療結束後第 12 週,血中仍偵測到病毒者)。(112/5/1)
|
| 注意事項 |
|
|
Epclusa 不可與其他含有sofosbuvir 成分的藥品併用。
|
| 過量處理 |
|
|
Epclusa 使用過量並無任何特定的解毒劑。如果用藥過量,應監視患者是否出現毒性反應的跡象。Epclusa 使用過量時的處置方式為一般的支持性措施,包括監視生命徵象,以及觀察患者的臨床狀態。血液透析可有效移除sofosbuvir 的主要循環代謝物 GS-331007,萃取率為53%。由於velpatasvir 會與血漿蛋白高度結合,因此血液透析不太可能達到明顯移除velpatasvir 的效果。
|
| 藥品保存方式 |
|
|
儲存在 25°C 以下。
|







































