| 結構式 |
|
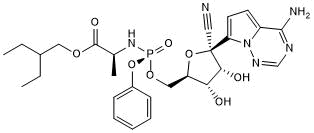
Remdesivir
(2S)-2-{(2R,3S,4R,5R)-[5-(4-Aminopyrrolo[2,1-f][1,2,4]triazin-7-yl)-5-cyano-3,4-dihydroxy-tetrahydro-furan-2-ylmethoxy]phenoxy-(S)-phosphorylamino}propionic acid 2-ethyl-butyl ester
|
| UpToDate |
UpToDate 連結
|
| 藥理作用 |
|
|
Remdesivir 是一種腺苷核苷酸前驅藥,會透過水解等作用代謝成單磷酸鹽形式的核苷類似物,然後分佈至細胞內,並代謝成具藥理活性的三磷酸鹽形式核苷類似物。此藥理活性代謝物會產生腺苷三磷酸(ATP)類似物的作用,並和天然ATP受質競爭,然後透過SARS-CoV-2 RNA依賴性RNA聚合酶的作用併入新生RNA鏈,從而導致病毒RNA複製期間的鏈終止作用延遲。此藥理活性代謝物對人類的DNA聚合酶α與β、RNA聚合酶II、粒線體DNA聚合酶γ 及粒線體RNA聚合酶的抑制作用(IC50 值)都> 200 μM。
|
| 適應症 |
|
重度新型冠狀病毒(SARS-CoV-2)感染症。
說明:重度之定義為在未使用吸氧治療下之血氧飽和度≤ 94%、須使用吸氧治療、須使用機械呼吸器、或已裝上葉克膜之病人。
|
| 用法用量 |
|
1.對成人與體重≥ 40 公斤的兒童,建議劑量為第1天IV 注射一劑remdesivir 200 毫克,然後從第2天起,每天一次IV 注射remdesivir 100毫克。
2.對體重介於3.5 公斤至< 40 公斤之間的兒童,建議依體重調整劑量,第1 天IV 注射一劑remdesivir 5毫克/ 公斤,然後從第2天起,每天一次IV 注射remdesivir 2.5毫克/公斤。
3.治療開始時已裝上葉克膜或機械呼吸器之病人,總治療時間最長為10天。
4.治療開始時未裝上葉克膜或機械呼吸器之病人為5 天,病情未獲改善時可延長,總治療時間最長為10天。
5.將本品加入生理食鹽水中,然後以30至120分鐘的時間靜脈輸注進入體內。
6.製備好的稀釋溶液不可與其他藥物合併投予。目前並不確知本藥與靜脈注射液及生理食鹽水以外之其他藥物的相容性。
7.由於VEKLURY不含防腐劑,因此,製備後的任何未使用的調製溶液及製備後的任何殘留調製溶液都應予以丟棄。
|
| 藥動力學 |
|
分佈
Remdesivir 的體外人類血漿蛋白結合率為87.9%。
代謝
Remdesivir 的代謝可能主要是透過水解酶之作用的媒介。
排泄
靜脈投予單劑量150 毫克以14C 標記的remdesivir 之後註),平均總回收劑量超過92%,其中分別約有74% 與18% 是在尿液和糞便中回收而得。在尿液中回收的remdesivir劑量大部份為核苷類似物(49%),並有10%是以remdesivir的形式回收。
註)目前核准的用法用量為第1天IV 輸注remdesivir 200毫克,然後從第2天起每天一次投予100毫克。
|
| 副作用 |
|
|
噁心、發燒、嘔吐。
|
| 交互作用 |
|
|
目前尚未於人體進行過remdesivir的藥物-藥物交互作用研究。
|
| 禁忌 |
|
|
曾對VEKLURY之任何組成產生過敏反應的病人。
|
| 注意事項 |
|
1.由於目前使用VEKLURY治療SARS-CoV-2 感染之療效與安全性方面的資訊極為有限,因此,應審慎評估使用的適當性,並將最新的資訊。
2.鑒於本藥大部份都是在臨床試驗中使用,VEKLURY原則上應使用於未使用吸氧治療下(room air)血氧飽和度≤ 94%、須吸氧治療、已裝上葉克膜(ECMO)、或已裝上侵入性機械呼吸器的SARS-CoV-2 感染重度病人。
|
| 警語 |
|
|
1.由於可能會發生急性腎功能損害,因此,在投予remdesivir 之前與之後都應每天進行腎功能檢查,嚴密監視病人的狀況。
2.由於可能會發生肝功能損害,因此,在投予remdesivir 之前與之後都應每天進行肝功能檢查,嚴密監視病人的狀況。
3.對體重介於3.5 公斤至< 40 公斤之間的兒童,僅能使用韋如意凍晶乾燥注射劑100毫克/瓶。
|
| 藥品保存方式 |
|
|
儲存於30℃以下。
|







































