| 結構式 |
|
|
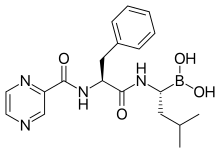
Bortezomib的化學結構式為:
[(1R)-3-methyl-1-({(2S)-3-phenyl-2-[(pyrazin-2-ylcarbonyl)amino]propanoyl}amino)butyl]boronic acid
|
| UpToDate |
UpToDate 連結
|
| 藥理作用 |
|
|
Bortezomib 是哺乳動物細胞內26S蛋白酶體(26S proteasome)類似胰凝乳蛋白酶活性 (chymotrypsinlike activity)的可逆性抑制劑。26S proteasome為一種很大的蛋白質複合物,會使有ubiquitinated標記的蛋白質降解。Ubiquitin-proteasome途徑在調節特定蛋白質的細胞內濃度上扮演著重要的角色,因此得以維持細胞內環境穩定。抑制26S 蛋白酶體可阻止此特殊的蛋白質分解過程,進而影響細胞內的多重訊息傳遞。瓦解正常內部環境穩定的機制可導致細胞死亡。在體外(in vitro)試驗已證實bortezomib對各種類型的癌細胞皆具細胞毒性。Bortezomib在體內(in vivo)非臨床腫瘤模型實驗中會延遲腫瘤生長,包括多發性骨髓癌。
|
| 適應症 |
|
1.Velcade可合併其他癌症治療藥品使用於未接受過治療的多發性骨髓瘤(Multiple myeloma)病人及曾接受過至少一種治療方式且已經接受或不適宜接受骨髓移植的進展性多發性骨髓癌病人。
2.被套細胞淋巴瘤Mantle Cell Lymphoma (MCL)病人。
|
| 用法用量 |
|
VELCADE 僅用於靜脈或皮下注射。切勿以其他方式投予VELCADE。
由於不同的給藥方式有不同的配製濃度,應謹慎計算給藥體積。 VELCADE的建議劑量為1.3mg/m2 。VELCADE 可以 1mg/mL的濃度靜脈注射給藥,或以 2.5mg/mL的濃度皮下注射給藥。
|
| 副作用 |
|
|
最常見的副作用為無力性症狀,如疲倦、不適、虛弱、噁心、腹瀉、嘔吐血小板減少及週邊神經病變等,不過大部分的副作用皆可以調整劑量的方式來作控制。
|
| 交互作用 |
|
強效CYP3A4誘導劑
與強效CYP3A4誘導劑併用會降低bortezomib的曝藥量,這可能會導致 VELCADE 的療效降低。應避免與強效CYP3A4誘導劑併用。
強效CYP3A4抑制劑
與強效CYP3A4抑制劑併用會增加Bortezomib曝藥量,這可能會升高發生 VELCADE 毒性反應的風險。因此,當Bortezomib 與強效CYP3A4抑制劑併用時應密切監測病人的 Bortezomib毒性徵狀及考慮減低Bortezomib的劑量。
|
| 禁忌 |
|
VELCADE 禁用於對Bortezomib、Boron或Mannitol 過敏的病人(不包含局部反應)。過敏性反應包含在內。
禁止將VELCADE以脊髓腔注射的方式給藥。將 VELCADE 以脊髓腔注射的方式給藥曾發生致死事件。
|
| 給付規定 |
|
9.28. Bortezomib(如Velcade):(96/6/1、98/2/1、99/3/1、99/9/1、100/10/1、101/6/1、105/5/1、109/4/1、109/6/1、111/1/1、112/4/1)附表九之三
限用於
1.合併其他癌症治療藥品使用於多發性骨髓瘤病人:(99/3/1、100/10/1、101/6/1、109/4/1、109/6/1、111/1/1、112/4/1)
(1) 每人終生以16個療程為上限。(99/9/1、109/4/1、109/6/1、111/1/1、112/4/1)
(2)需經事前申請後使用,每次申請4個療程。(101/6/1)
(3) 開始治療時病患須同時符合下列Ⅰ.與Ⅱ.的條件:(112/4/1)
Ⅰ.骨髓漿細胞(plasma cells)比例≧10%,或是經切片確認且有≧1顆的plasmacytoma。
Ⅱ.出現下列任一臨床症狀:
?.腎功能不全:serum creatinine>2.0mg/dL或estimated GFR (eGFR)<40 ml/min,且無其他原因可以解釋。
?.高血鈣(corrected serum calcium>11.0 mg/dL 或 2.75 mmol/L)。
iii.貧血(Hemoglobin<10 gm/dL且無其他原因可以解釋)。
iv.影像檢查確認之osteolytic bone lesion(s)。
v.骨髓漿細胞(plasma cells)比例≧60%。
vi.Serum free light-chain ratio≧100。
(4)使用4個療程後,必須確定藥物使用後paraprotein (M-protein)未上升 (即表示為response或stable status),或對部分non-secretory type MM病人以骨髓檢查plasma cell之比率為療效依據,方可繼續使用。(101/6/1、109/4/1)
(5)若病患於前線療程符合前項規定(4)之療效而醫師決定可暫時停藥,則後續療程可保留,於疾病復發時,再行申請使用。(101/6/1、109/4/1)
(6) 112年3月31日以前已核定用藥之病人,得經事前審查核准後,使用至總療程上限(即終生16個療程)或使用期間發生疾病惡化為止。(112/4/1)
2.被套細胞淋巴瘤(Mantle Cell Lymphoma, MCL)病人:(98/2/1、105/5/1)
(1)每人以8個療程為上限。(99/9/1)
(2)每日最大劑量1.5mg/m2/day;每個療程第1,4,8,11日給藥。
(3)第一線使用過復發者,不得申請再次使用。(105/5/1)
(4)需經事前審查核准後使用。
|
| 過量處理 |
|
目前尚未有VELCADE 過量的特定解毒劑。在人類,使用超過兩倍建議治療劑量時,曾通報過與症狀性低血壓急性發作以及血小板過低相關的死亡案例。
發生過量時,應監測病人的生命徵象並給予適當的支持性照護。
|
| 藥品保存方式 |
|
|
當避光儲存於原包裝中,VELCADE 在包裝上所記載的有效期限內可被穩定地儲存。 VELCADE 並無添加抗菌防腐劑,配製過後的 VELCADE 溶液應在八小時內使用完畢,當依指示配製時,VELCADE 可以儲存於25ºC。配製後之溶液在輸注前可以儲存於原包裝的小瓶內或是注射針筒中,在注射針筒中可以儲存長達八小時,然而,當曝露在室內光線下,總儲存時間不得超過八小時。
|







































