| 結構式 |
|
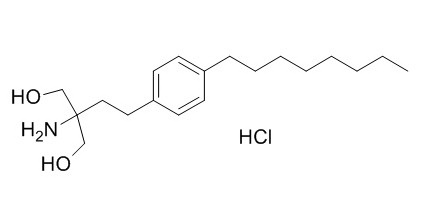
Fingolimod
|
| UpToDate |
UpToDate 連結
|
| 藥理作用 |
|
|
Fingolimod 是由鞘氨酸激酶(sphingosine kinase) 代謝成活性代謝物fingolimod phosphate。Fingolimod-phosphate 是一種鞘氨酸1- 磷酸鹽(sphingosine 1- phosphate,S1P) 受體調節劑,與鞘氨酸1- 磷酸鹽受體1、3、4 結合具有很高的親和力。Fingolimod- phosphate 阻斷淋巴球自淋巴結中移出的能力,減少週邊血的淋巴球數。Fingolimod 對多發性硬化症產生治療作用的機轉未明,但可能和減少淋巴球細胞滲透至中樞神經系統中有關。
|
| 適應症 |
|
|
復發型多發性硬化症( 前一年有一次復發或前兩年有兩次復發者)。
|
| 用法用量 |
|
建議劑量為每日口服一顆0.5 毫克Gilenya 膠囊。Fingolimod 劑量高於0.5 毫克時,可能會產生更多的不良反應,而沒有額外的效益。
Gilenya 可單獨或與食物併服。
|
| 藥動力學 |
|
吸收
Fingolimod 達到最高血中濃度的時間(Tmax) 為12 ~ 16 小時。擬似絕對口服生體可用率為93%。
與食物併服不會改變fingolimod 或fingolimod- phosphate 的最高血中濃度(Cmax) 或暴露量(AUC)。因此,服用Gilenya 時無須考量用餐與否。
每天服藥1 - 2 個月後會達到穩定狀態血中濃度,且穩定狀態下濃度大約是開始服用第一劑時的10 倍。
分佈
Fingolimod 大量分佈在紅血球內(86%)。少量的fingolimod- phosphate (<17%)被血球細胞攝入。Fingolimod 及fingolimod- phosphate 和血漿蛋白結合超過99.7%。
代謝
Fingolimod 主要經由人類CYP4F2 同功酶代謝,少部份經由CYP2D6,2E1,3A4 和4F12 代謝。這些同功酶的抑制劑或誘導劑可能會改變fingolimod 或fingolimod-phosphate 的暴露量。Fingolimod 的氧化作用涉及多個CYP 同功酶,顯示使用單一特定的CYP 同功酶抑制劑對fingolimod 的代謝不會有明顯的抑制作用。
排除
Fingolimod 的血液清除率為6.3 ± 2.3 L/h,平均擬似末相半衰期(t1/2) 為6 - 9天。在末相,fingolimod 和fingolimod phosphate 血中濃度呈現平行下降速度之現象,顯示兩者具相似的半衰期。
在口服後,約81% 的劑量會以非活性代謝物形式緩慢地排泄至尿液中。
Fingolimod 與fingolimod- phosphate 都不會完整地排泄至尿液中,但卻為糞便排泄的主要組成且兩者含量皆低於投藥量的2.5%。
|
| 副作用 |
|
|
頭痛、流行性感冒、腹瀉、背痛、肝臟酵素濃度上升、和咳嗽。
|
| 交互作用 |
|
Ketoconazole
與ketoconazole 併用時,fingolimod 和fingolimod-phosphate 的血中濃度會增加1.7 倍。病人併用Gilenya 和全身性ketoconazole 治療時,應嚴密監測,因為發生不良反應的風險更高。
|
| 禁忌 |
|
1.在過去六個月中,曾發生心肌梗塞、不穩定型心絞痛、中風、短暫性缺血性中風(TIA)、代償不良之心臟衰竭且需要住院、或第III/IV 級心臟衰竭的病人。
2.曾經有過或現有第二度Mobitz 第II 型或第三度房室傳導阻斷或病竇症候群,除非病人有裝設心律調節器。
3. QTc 間隔基期值≥500ms。
4.接受Ia 類或III 類抗心律不整藥物治療。
5.已知免疫不全症候群。
6.會增加伺機性感染風險的病人,包括免疫抑制病人(包括正在接受免疫抑制劑治療或以前次治療產生的免疫抑制)。
7.嚴重的活動性感染,慢性活動性感染(肝炎,肺結核)。
8.嚴重活性惡性腫瘤,除了表皮基細胞癌病人以外。
9.嚴重肝功能不全(Child-Pugh Class C)。
10.對主成分或其他賦形劑成分過敏。
|
| 給付規定 |
|
8.2.3.5.Fingolimod(如Gilenya):(101/9/1、102/10/1、109/1/1、109/10/1)
1.限用於雖已接受乙型干擾素或glatiramer治療,相較於前一年度復發?仍不變或反而上升之高度活躍型復發緩解之多發性硬化症病人(highly active relapsing–remitting multiple sclerosis 即 前一年有一次以上復發或是前兩年有兩次以上復發),但排除使用於:
(1)EDSS (Expanded Disabi1ity Status Scale)大於5.5之患者。
(2)視神經脊髓炎(neuromyelitis optica,NMO),包括:
Ⅰ有視神經及脊髓發作。
Ⅱ出現下列2 種以上症狀:
i.脊髓侵犯大於3節;
ii.NMO-IgG or Aquaporin-4 抗體陽性;
iii.腦部磁振造影不符合多發性硬化症診斷標準。
2.須經事前審查核准後使用,每年需重新申請,併應提出整個用藥期間的復發情形。(102/10/1)
3.使用兩年後,年度復發率(average annual relapse)無法減少※時應停止本藥品之治療。(102/10/1)
4.個案在停藥觀察期間復發且為高度活躍型復發緩解之多發性硬化症病人(highly active relapsing– remitting multiple sclerosis可再申請並經事前審查核准後使用。(102/10/1)
※年度復發率無法減少之定義:
採計使用fingolimod藥物後一年至兩年復發次數之數據 (以最近一年或兩年之復發次數除以1或2來計算),較諸更先前一年或兩年之年復發率皆無再減少時。(102/10/1)
|
| 警語 |
|
|
因為具有心搏過緩和房室傳導阻斷的風險,開始使用Gilenya 治療時,應監測病人。
|
| 藥品保存方式 |
|
|
儲存於 30℃以下。
|







































