| 結構式 |
|
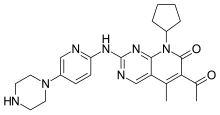
Palbociclib
|
| UpToDate |
UpToDate 連結
|
| 藥理作用 |
|
|
Palbociclib是一種具高度選擇性及可逆性的週期素依賴性激酉每(CDK) 4和6的抑制劑。週期素D1和CDK4/6是多種會導致細胞增生之訊息傳遞路徑的下游。
|
| 適應症 |
|
1. 對於荷爾蒙受體為陽性、第二型人類表皮生長因子接受體(HER2) 呈陰性之局部晚期或轉移性乳癌之停經後婦女,IBRANCE可與芳香環轉化酶抑制劑(aromatase inhibitor)合併使用。
2. 對於雌激素受體為陽性、第二型人類表皮生長因子接受體(HER2) 呈陰性之局部晚期或轉移性乳癌之婦女,IBRANCE可合併fulvestrant 用於先前曾接受過內分泌治療者。
|
| 用法用量 |
|
劑量:
建議劑量為125毫克palbociclib每日一次,連續治療21天後停止治療7天(3/1療程),以28天為一個完整的週期。只要患者可獲得臨床效益,即應持續使用IBRANCE治療,或持續治療至出現無法接受的毒性反應為止。
用法:
IBRANCE僅供口服使用。本品應與食物併服,最好是於用餐時服用,以確保palbociclib的暴露量維持一致。
IBRANCE膠囊應整顆吞服(吞服前請勿咀嚼、咬碎或打開膠囊)。
|
| 藥動力學 |
|
吸收
通常可於口服投予後6至12小時觀察到palbociclib的平均Cmax。口服一劑125毫克之palbociclib後的平均絕對生體可用率為46%。
分佈
體外試驗顯示,palbociclib與人類血漿蛋白的結合率為~85%,且不具濃度依賴性。
生物轉化
體外和體內試驗顯示,palbociclib在人體內會進行廣泛的肝臟代謝。對人類口服投予單劑125毫克的[14C] palbociclib之後,palbociclib的主要代謝途徑包括氧化與硫酸化,次要途徑包括醯化與葡萄糖醛酸化。Palbociclib為血漿中的主要循環化合物。
排除
在晚期乳癌患者中,palbociclib的幾何平均廓清率(CL/F)為63升/小時,平均血漿排除半衰期為28.8小時。
|
| 副作用 |
|
|
嗜中性白血球減少症、白血球減少症、貧血、血小板減少症、食慾降低、口腔炎、噁心、嘔吐、腹瀉、皮疹、禿髮、疲倦。
|
| 交互作用 |
|
Palbociclib主要是透過CYP3A及磺基轉移酶 (SULT) SULT2A1的作用進行代謝。體內試驗顯示,palbociclib是一種弱效的時間依賴性CYP3A抑制劑。
其他藥物對palbociclib之藥物動力學的影響
CYP3A抑制劑的影響
和僅投予單劑125毫克的palbociclib相比較,將多劑量的200毫克
itraconazole與單劑125毫克的palbociclib合併投予會使palbociclib的總暴露量(AUCinf)與尖峰濃度(Cmax)分別升高約87%與34%。
CYP3A誘導劑的影響
和僅投予單劑125毫克的palbociclib相比較,將多劑量600毫克的rifampin與單劑125毫克的palbociclib合併投予會使palbociclib的AUCinf與Cmax分別降低85%與70%。
|
| 禁忌 |
|
1. 對活性成分或本膠囊中所列之任何賦形劑過敏。
2. 使用含有聖約翰草成分(St. John’s Wort)(或稱金絲桃草)的製劑。
|
| 給付規定 |
|
9.72.CDK4/6抑制劑 (如 palbociclib):(108/10/1、108/12/1、109/4/1、109/10/1、110/5/1、110/10/1、113/1/1)
1. 用於停經後乳癌婦女發生遠端轉移後之全身性藥物治療,須完全符合以下條件:(109/10/1、110/5/1、110/10/1、113/1/1)
(1)荷爾蒙接受體為:ER或PR >30%。(109/10/1、113/1/1)
(2)HER-2 檢測為陰性。
(3)經完整疾病評估後未出現器官轉移危急症狀 (visceral crisis)且無中樞神經系統(CNS)轉移。(110/10/1)
(4)骨轉移不可為唯一轉移部位。(110/10/1)
(5)病患目前未接受卵巢功能抑制治療 (包含GnRH analogue等) 且滿足下列條件之一:(110/5/1)
Ⅰ.年齡滿55歲。
Ⅱ.曾接受雙側卵巢切除術。
Ⅲ.FSH及estradiol血液檢測值在停經後數值範圍內。
2.用於停經前/正在停經乳癌婦女發生遠端轉移後之全身性藥物治療,須與芳香環轉化?抑制劑及GnRH analogue併用。(113/1/1)
(1)荷爾蒙接受體為:ER或PR >30%。
(2)HER-2 檢測為陰性。
(3)經完整疾病評估後未出現器官轉移危急症狀 (visceral crisis)且無中樞神經系統(CNS)轉移。
(4)骨轉移不可為唯一轉移部位。
3.經事前審查核准後使用,核准後每24週須檢附療效評估資料再次申請,若疾病惡化即必須停止使用,且後續不得再申請使用本類藥品。(110/10/1)
4.使用限制:
(1)ribociclib每日最多處方3粒。
(2)palbociclib每日最多處方1粒。
(3)本類藥品僅得擇一使用,唯有在耐受不良時方可轉換使用,使用總療程合併計算,以每人終生給付24個月為上限。
5.110年9月30日以前已核定用藥之病人,得經事前審查核准後,使用至總療程(即終生24個月)或總療程期間疾病惡化為止,且後續不得再申請使用本類藥品。(110/10/1、113/1/1)
6.若先前使用everolimus無效後,不得再申請本類藥品。(109/4/1)
|
| 注意事項 |
|
1. Palbociclib不可與 葡萄柚或葡萄柚汁併服。
2. IBRANCE可能會導致疲倦,因此,患者在駕駛或操作機械時應謹慎。
3. 本品含有乳醣成分。有半乳糖不耐症、Lapp乳糖酉每缺乏症或葡萄糖- 半乳糖吸收不良等罕見遺傳問題的患者不可使用本藥。
|
| 飲食提示 |
|
|
Palbociclib不可與葡萄柚或葡萄柚汁併服。
|
| 警語 |
|
IBRANCE對駕駛及操作機械之能力的影響極微。不過,IBRANCE可
能會導致疲倦,因此,患者在駕駛或操作機械時應謹慎。
|
| 過量處理 |
|
|
如果palbociclib使用過量,可能會發生胃腸道(如噁心、嘔吐)和血液學 (如嗜中性白血球減少症)毒性反應,因此應採取一般的支持性照護措施。
|
| 藥品保存方式 |
|
|
請儲存於30°C以下。
|







































