| 結構式 |
|
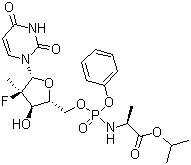
Sofosbuvir
Isopropil (2S)-2-[[[(2R,3R,4R,5R)-5-(2,4-diossopirimidin-1-il)-4-fluoro-3-idrossi-4-metil-tetraidrofuran-2-il]metossi-fenossi-fosforil]amino]propanoato
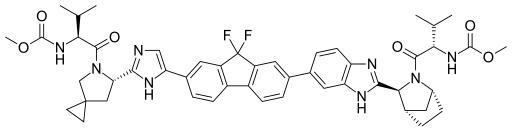
Ledipasvir
Methyl N-[(2S)-1-[(6S)-6-[5-[9,9-Difluoro-7-[2-[(1S,2S,4R)-3-[(2S)-2-(methoxycarbonylamino)-3-methylbutanoyl]-3-azabicyclo[2.2.1]heptan-2-yl]-3H-benzimidazol-5-yl]fluoren-2-yl]-1H-imidazol-2-yl]-5-azaspiro[2.4]heptan-5-yl]-3-methyl-1-oxobutan-2-yl]carbamate
|
| UpToDate |
UpToDate 連結
|
| 藥理作用 |
|
|
HARVONI是一種含有ledipasvir與sofosbuvir成分的固定劑量複方藥物,這兩種成分皆為可對抗C型肝炎病毒的直接作用型抗病毒劑。
|
| 適應症 |
|
|
HARVON(I 併用或未併用ribavirin)適用於治療患有慢性C型肝炎病毒(hepatitis C virus, HCV)基因型1、4、5或6感染症的患者。
|
| 用法用量 |
|
|
HARVONI 的建議劑量為每日一次口服一顆錠劑,可與食物併服亦可不與食物併服。
|
| 藥動力學 |
|
|
吸收
曾針對健康成人受試者與患有慢性C型肝炎的受試者評估ledipasvir、sofosbuvir及其主要循環代謝物GS-331007的藥物動力學特性。口服投予HARVONI之後,可於投藥後4-4.5小時(中位數)觀察到ledipasvir的最高血中濃度。Sofosbuvir會快速被吸收進入體內,並可於投藥後~0.8-1小時(中位數)觀察到最高血中濃度。GS-331007的最高血中濃度則是出現於投藥後3.5至4小時(中位數)。
分佈
Ledipasvir與人類血漿蛋白的結合率約為>99.8%。
Sofosbuvir與人類血漿蛋白的結合率約為61-65%,且在1 μg/mL至20 μg/mL的範圍內,此結合作用並不會受到藥物濃度的影響。
代謝
在體外試驗中,並未發現任何明顯的ledipasvir透過人類CYP1A2、CYP2C8、CYP2C9、CYP2C19、CYP2D6及CYP3A4酵素進行代謝的現象。
Sofosbuvir會在肝臟進行廣泛的代謝,形成具藥理活性的核苷類似物三磷酸鹽GS-461203。其代謝活化途徑包括由人類組織蛋白酶A (CatA)或羧酸酯酶1 (CES1)所催化的羧酸酯基團連續水解作用,以及組氨酸三聯體核苷酸結合蛋白1 (HINT1)的胺基磷酸酯裂解作用,之後再透過嘧啶核苷酸生物合成途徑進行磷酸化作用。
排除
口服單劑90毫克的[14C]- ledipasvir之後,糞便與尿液中的[14C]放射活性平均總回收量約為87%,大部份的放射活性劑量是自糞便回收而得(約86%)。
口服單劑400毫克的[14C]-sofosbuvir之後,平均總回收劑量大於92%,其中分別約有80%、14%與2.5%是自尿液、糞便與呼氣中回收而得。
|
| 副作用 |
|
|
疲倦與頭痛。
|
| 交互作用 |
|
|
Ledipasvir與sofosbuvir皆為藥物運輸蛋白P-gp及乳癌抗藥蛋白(BCRP)的作用受質,而GS-331007則不是。P-gp誘導劑(如rifampin或聖約翰草)可能會降低ledipasvir與sofosbuvir的血中濃度,從而導致HARVONI的治療效果減弱,因此不建議將P-gp誘導劑與HARVONI併用。
|
| 禁忌 |
|
|
無。
|
| 給付規定 |
|
10.7.9.Sofosbuvir(如Sovaldi)(107/1/1、107/6/1、108/1/1、108/6/1、109/1/1、109/7/1):
1.限用於成人慢性病毒性C型肝炎患者,並依據「C型肝炎全口服新藥健保給付執行計畫」辦理。(109/1/1、109/7/1)
2.限使用於HCV RNA為陽性及無肝功能代償不全之病毒基因型第2型成人病患。(107/6/1、108/1/1、108/6/1)
3.需合併ribavirin治療,每人給付療程12週,醫師每次開藥以4週為限。(108/1/1)
4.限未曾申請給付其他同類全口服直接抗病毒藥物(direct-acting anti-viral, DAAs),且不得併用其他DAAs。
|
| 注意事項 |
|
|
不建議將HARVONI 與其他含有sofosbuvir成分的產品
(SOVALDI)併用。
|
| 警語 |
|
不建議將amiodarone與HARVONI合併投予。對正在使用amiodarone且無任何其他可替代之有效治療選擇的患者,當準備合併投予HARVONI時:
1. 應告知患者發生嚴重症狀性心搏徐緩的風險
2. 建議在合併投藥的最初48小時應住院進行心臟監測,之後至少在最初2週治療期間應每天回診監測或自行監測心跳速率。
|
| 過量處理 |
|
|
HARVONI使用過量並無任何特定的解毒劑。如果使用過量,應監視患者是否出現毒性反應的跡象。HARVONI使用過量時的處置方式為一般的支持性措施,包括監測生命徵象與觀察患者的臨床狀態。由於ledipasvir會與血漿蛋白高度結合,因此血液透析可能無法將ledipasvir有效移除。血液透析可有效移除sofosbuvir的主要循環代謝物GS-331007,移除率為53%。
|
| 藥品保存方式 |
|
|
請保存於25℃以下陰涼乾燥處。
|







































