| 結構式 |
|
|
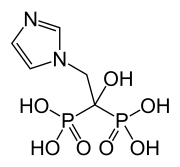
Zoledronic acid
(1-hydroxy-2-imidazol-1-yl-1-phosphono-ethyl)phosphonic acid
|
| UpToDate |
UpToDate 連結
|
| 藥理作用 |
|
Aclasta屬於含氮的雙磷酸鹽類化合物,主要作用在骨骼。它是蝕骨細胞骨質再吸收作用的抑制劑。
雙磷酸鹽類化合物對骨骼的選擇性作用是因為對礦質化骨骼具有高親和性。Zoledronic acid以靜脈給藥方式可快速分佈至骨骼中,如同其他雙磷酸鹽類化合物,具骨質再吸收部位的局部優先選擇性。Zoledronic acid在蝕骨細胞中的主要分子標的為酵素的焦磷酸酯合成酶(farnesyl pyrophosphate synthase) 。Zoledronic acid之相對長作用周期,使得其與骨鈣質具高結合率。
|
| 適應症 |
|
1. 治療停經後婦女的骨質疏鬆症,以降低發生髖關節、脊椎與非脊椎性骨折的機率,並增加骨密度。
2. 預防停經後婦女的骨質疏鬆症。
3. 適用於治療男性骨質疏鬆症,以增加骨密度。
4. 適用於治療及預防發生於男性與女性之類固醇性骨質疏鬆症;這些病患為剛開始使用或持續使用每日劑量相當於7.5 mg prednisone或更高劑量的全身性類固醇,且預期將持續使用類固醇至少12個月者。
5. 骨佩吉特氏病(Paget’s disease of bone) Aclasta治療發生於男性與女性的骨佩吉特氏病(Paget’s disease of bone)。治療血清鹼性磷酸酶高於正常年齡參考值兩倍以上、具症狀或有併發症危險的骨佩吉特氏病病人。
|
| 用法用量 |
|
1. 建議劑量為每年單次靜脈輸注5mg輸注液,輸注時間不得少於15分鐘,以固定的輸注速率給藥。
2. 在靜脈輸注之後,應以10mL生理食鹽水沖洗靜脈管線。
3. Aclasta注射液不得接觸到任何含鈣離子或其他含二價離子的溶液,須以單獨的輸注管以單次注射液給藥。
|
| 藥動力學 |
|
|
分佈:
在輸注後24小時,由輸注結束時的最高濃度遽降至低於Cmax的1%,族群半衰期為t1/2α 0.24小時,藥物排除初期的半衰期為t1/2β 1.87小時。
代謝:
Zoledronic acid無法在試管試驗內抑制人類P450酵素。Zoledronic acid在體內試驗中不會歷經生物轉化。在動物研究中,存在於糞便中的劑量< 3%的靜脈注射劑量,與存在於尿中或被骨骼佔用的量相當,這表示藥物是經由腎臟完整排除。
分泌:
64名癌症與骨轉移患者在24小時內,平均(± S.D.)有39 ± 16%的zoledronic acid注射劑量出現在尿液中,在投藥後第2天,在尿中只能發現微量的藥物。藥物排至尿中的0-24小時累積百分比不受劑量支配。0-24小時內未在尿中發現藥物餘量,表示藥物可能與骨骼相結合,而緩慢地釋回,進入全身循環內,造成低血中濃度的時間延長。Zoledronic acid的0-24小時腎清除率為3.7 ± 2.0 L/小時。
|
| 副作用 |
|
|
類流感疾病、發熱、關節痛、肌痛、頭痛。
|
| 交互作用 |
|
|
未針對Aclasta進行體內藥物交互作用試驗。
|
| 禁忌 |
|
Aclasta禁用於下列病患:
1. 低血鈣症。
2. Aclasta禁用於肌酸酐清除率< 35ml/min 以及證實具有急性腎功能不全的病患,因為這些病患發生腎衰竭的風險較高。
3. 已知對zoledronic acid或Aclasta所含任何成分過敏。過敏反應包括少見的蕁麻疹和血管性水腫,以及非常罕見的過敏性反應/休克案例報告。
|
| 給付規定 |
|
5.5.3.2.2.Zoledronic acid 5mg (如Aclasta 5mg/100mL Solution for infusion)( 98/6/1、100/1/1)
用於變形性骨炎(Paget's disease)
5.6.骨質疏鬆症治療藥物(100/1/1)
5.6.1抗骨質再吸收劑(anti- resorptive)(101/3/1、101/5/1、102/2/1、102/8/1、103/2/1、103/10/1、104/8/1、106/12/1)
1.藥品種類
(1) zoledronate 5mg (如Aclasta 5mg/100mL solution for infusion)、
2.使用規定
(1)限用於停經後婦女(alendronate、zoledronate、denosumab及risedronate 35mg亦可使用於男性,risedronate 150mg不可使用於男性)因骨質疏鬆症(須經DXA 檢測BMD之T score≦ -2.5SD)引起脊椎或髖部骨折,或因骨質疏少症(osteopenia)(經DXA檢測BMD之-2.5SD (2)治療時,一次限用一項藥物,不得併用其他骨質疏鬆症治療藥物。
(3)使用雙磷酸鹽類藥物,須先檢測病患之血清creatinine濃度,符合該項藥物仿單之建議規定。
|
| 注意事項 |
|
1. 開始雙磷酸鹽類治療前,應進行例行的口腔檢查。
2. 若注射液已冷藏,在輸注前先讓冷藏溶液回復到室溫。打開瓶裝後,溶液在2-8°C的溫度下可保持24小時。
|
| 警語 |
|
|
Aclasta所含的活性成分與使用於腫瘤適應症之Zometa相同,接受Zometa治療的病患不應再接受Aclasta治療。
|
| 過量處理 |
|
目前對於以zoledronic acid (Aclasta)溶液進行靜脈輸注的急性藥物過量的臨床經驗有限。對於使用高於建議劑量的病患,應仔細地監測。劑量過高可能會造成臨床上明顯的腎功能不全、低血鈣症、低磷酸鹽血症及低血鎂症。血中鈣、磷酸鹽及鎂的臨床相關濃度降低,應分別以靜脈注射葡萄糖酸鈣、鉀或磷酸氫二鈉及硫酸鎂來作矯正。
Aclasta的單一劑量不應超過5mg,輸注時間不得少於15分鐘。
|
| 藥品保存方式 |
|
|
儲存條件為15-30°C。
|







































