|
|
|
|
| 本網頁資料僅供參考,如有疑問或錯誤請仍依廠商資料為主。 |
| 醫令碼 |
20907 |
健保碼 |
BC27323100 |
| 商品名 |
MAVIRET 100MG/40MG(健保) |
藥品許可證 |
衛部藥輸字第027323號 |
| 中文名 |
艾百樂膜衣錠 |
健保局藥理類別 |
|
| 學名 |
Glecaprevir+Pibrentasvir |
外觀描述 |
|
| 類別 |
PHR |
劑量 |
TAB |
| 抗生素 |
|
管制藥 |
|
| 仿單 |
20907 MAVIRET 100MG/40MG(健保)
|
| 用藥指導單張 |
 |
| 結構式 |
|

Glecaprevir 成分:
Glecaprevir 化學名為 (3aR,7S,10S,12R,21E,24aR)-7-tert-butyl-N-{(1R,2R)-2-(difluoromethyl)-1- [(1-methylcyclopropane-1-sulfonyl)carbamoyl]cyclopropyl}-20,20-difluoro-5,8-dioxo2,3,3a,5,6,7,8,11,12,20,23,24a-dodecahydro-1H,10H-9,12- methanocyclopenta[18,19][1,10,17,3,6]trioxadiazacyclononadecino[11,12-b]quinoxaline-10- carboxamide hydrate。
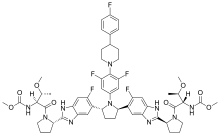
Pibrentasvir 成分:
Pibrentasvir 化學名為 Methyl {(2S,3R)-1-[(2S)-2-{5-[(2R,5R)-1-{3,5-difluoro-4-[4-(4- fluorophenyl)piperidin-1-yl]phenyl}-5-(6-fluoro-2-{(2S)-1-[N-(methoxycarbonyl)-O-methyl-Lthreonyl]pyrrolidin-2-yl}-1H-benzimidazol-5-yl)pyrrolidin-2-yl]-6-fluoro-1H-benzimidazol-2- yl}pyrrolidin-1-yl]-3-methoxy-1-oxobutan-2-yl}carbamate。
|
| UpToDate |
UpToDate 連結
|
| 藥理作用 |
|
|
MAVIRET 是 glecaprevir 和 pibrentasvir 固定劑量複方製劑,兩種成分都是直接作用於 C 型肝炎病毒的抗病毒藥物。
|
| 適應症 |
|
|
MAVIRET 適用於治療成人慢性 C 型肝炎病毒 (HCV) 基因型 1、2、3、4、5、或 6 之感染。
|
| 用法用量 |
|
|
MAVIRET 的口服建議劑量是每日一次,隨餐服用三顆錠劑, (每日總劑量:glecaprevir 300 mg,pibrentasvir 120 mg)。
|
| 藥動力學 |
|
|
如仿單所示。
|
| 副作用 |
|
|
最常見不良反應 (不論等級) 包括頭痛、倦怠和噁心。
|
| 交互作用 |
|
|
Carbamazepine、efavirenz 和金絲桃草可能顯著降低 glecaprevir 和 pibrentasvir 的血中濃度,因而減低 MAVIRET 的治療效果。這些不建議與 MAVIRET 併用。
|
| 禁忌 |
|
1. 已知會對活性成分或對任何第 11 節的賦形劑產生過敏反應。 2.MAVIRET 禁用於重度肝功能不全的患者 (Child-Pugh C)。
3. MAVIRET 禁止與 含 atazanavir 製劑, simvastatin, dabigatran etexilate, 含 ethinyl oestradiol 製劑, rifampicin 併用。
|
| 給付規定 |
|
10.7.10.Glecaprevir/pibrentasvir(如Maviret)(107/8/1、108/1/1、108/6/1、109/1/1、109/4/1、109/7/1、109/8/1、110/6/1、111/2/1):
1.限用於成人慢性病毒性C型肝炎患者,並依據「C型肝炎全口服新藥健保給付執行計畫」辦理。(109/1/1、109/7/1)
2.限使用於HCV RNA為陽性及無肝功能代償不全之病毒基因型第1型、第2型、第3型、第4型、第5型或第6型12歲以上病患。(108/1/1、108/6/1、109/8/1、111/2/1)
3.給付療程如下,醫師每次開藥以4週為限。(108/1/1、109/4/1、110/6/1)
(1)未曾接受治療之患者,給付8週。(109/4/1、109/8/1)
(2)曾接受含(peg)interferon及ribavirin及合併或不合併sofosbuvir治療組合之患者:(110/6/1)
Ⅰ.基因型第1、2、4、5或6型:
i.無肝硬化者,給付8週。
ii.具代償性肝硬化(Child-Pugh score A)者,給付12週。
Ⅱ.基因型第3型,且無肝硬化或具代償性肝硬化(Child-Pugh score A)者,給付16週。
(3)曾接受含NS5A抑制劑或NS3/4A蛋白?抑制劑治療之基因型第1型患者:
Ⅰ.若曾接受NS3/4A蛋白?抑制劑治療,但未曾接受NS5A抑制劑治療者,給付12週。
Ⅱ.若曾接受NS5A抑制劑治療,但未曾接受NS3/4A蛋白?抑制劑治療者,給付16週。
4.限未曾申請給付其他同類全口服直接抗病毒藥物(direct-acting anti-viral, DAAs),且不得併用其他DAAs,惟若符合下列情形之一者,可再治療一次(一個療程):(110/6/1)
(1)接受本項藥品或其他DAAs第一次治療時中斷療程,且中斷原因屬專業醫療評估必須停藥者。
(2)接受本項藥品或其他DAAs第一次治療結束後第12週,血中偵測不到病毒,目前血中又再次偵測到病毒者。
(3)接受其他DAAs第一次治療,於治療完成時或治療結束後第12週,血中仍偵測到病毒者,或治療4週後之病毒量未能下降超過二個對數值(即下降未達100倍)發生在108年1月1日前者。
|
| 過量處理 |
|
|
藥過量時應監測患者是否有毒性徵兆或症狀,必要時應立刻施予適當的症狀治療。 Glecaprevir 和 pibrentasvir 無法經由血液透析大量移除。
|
| 藥品保存方式 |
|
|
儲存於 30°C (86°F) 以下。
|
|
|







































