| 結構式 |
|
|
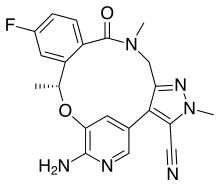
Lorlatinib
(10R)-7-amino-12-fluoro-2,10,16-trimethyl-15-oxo-10,15,16,17-tetrahydro-2H-4,8-methenopyrazolo[4,3-h][2,5,11]
benzoxadiazacyclotetradecine-3-carbonitrile。
|
| UpToDate |
UpToDate 連結
|
| 藥理作用 |
|
Lorlatinib 是一種激酶抑制劑,對 ALK 和 ROS1 以及TYK1、FER、FPS、TRKA、TRKB、TRKC、FAK、FAK2 和 ACK 具有體外活性。Lorlatinib 展現出對抗ALK 酶多種突變形式的體外活性,包括在接受crizotinib 和其他 ALK 抑制劑給藥出現疾病惡化時,於腫瘤中所檢測到的一些突變。
在皮下植入帶有融合EML4 與 ALK 變體 1 或 ALK 突變體(包括在接受 ALK抑制劑給藥出現疾病惡化時於腫瘤中檢測到的 G1202R 和 I1171T 突變體)腫瘤的鼷鼠中,投予lorlatinib 會產生抗腫瘤活性。在顱內植入 EML4‑ALK 所驅動之腫瘤細胞株的鼷鼠中,Lorlatinib 亦展現出抗腫瘤活性,並延長鼷鼠的存活時間。在體內模型中,lorlatinib 的總體抗腫瘤活性具劑量依賴性,並與 ALK 磷酸化的抑制相關。
|
| 適應症 |
|
|
LORVIQUA 適用於ALK 陽性之晚期非小細胞肺癌(NSCLC)病人在使用(1)crizotinib 和後續至少一種其他的ALK 抑制劑或(2) 以alectinib 或ceritinib 做為第一種ALK 抑制劑治療非小細胞肺癌發生惡化。
|
| 用法用量 |
|
LORVIQUA 的建議劑量為口服100毫克,每日一次,可伴隨或不伴隨食物服用,直到疾病惡化或發生無法耐受的毒性。
錠劑應整粒吞服。請勿咀嚼、磨碎或剝半
|
| 藥動力學 |
|
吸收
單次口服100 毫克和每日一次口服100 毫克達穩定狀態後的 lorlatinib 之Tmax 中位數,分別為 1.2 小時(0.5 至 4 小時)和 2 小時(0.5 至 23 小時)。
與靜脈內給藥相比,口服給藥的平均絕對生體可用率為 81%(90% CI 為75.7%,86.2%)。
食物的影響
隨高脂肪、高熱量餐(大約含1000 卡路里,其中 150 卡來自蛋白質、250 卡來
自碳水化合物及 500 至 600 卡來自脂肪)給與LORVIQUA 後,食物對 lorlatinib
的藥物動力學不具臨床意義的影響。
分布
在體外試驗中,lorlatinib 濃度在 2.4 μM 時的血漿蛋白結合率為 66%。血液對比血漿的比值為 0.99。在單次靜脈注射劑量後,平均(CV%)穩定狀態分佈體積(Vss)為305 L(28%)。
排除
單次口服 LORVIQUA 100 毫克後,lorlatinib 的平均血漿半衰期(t½)為 24 小時(40%)。單次口服100 毫克後的平均口服清除率(CL/F)為每小時 11 公升(35%),穩定狀態時增加至每小時 18 公升(39%),顯示存在自身誘導。
代謝
在體外試驗中,lorlatinib 主要由 CYP3A4 與 UGT1A4 代謝,少部分由 CYP2C8、CYP2C19、CYP3A5 與 UGT1A3 代謝。
排泄
單次口服100 毫克放射性標記 lorlatinib 後,在尿中回收48%的放射性活性物質(未改變形式占< 1%),41% 於糞便中回收(未改變形式約有9%)。
|
| 副作用 |
|
|
最常見的不良反應為水腫、周邊神經病變、高膽固醇血症、認知影響、呼吸困難、疲倦、體重增加、關節痛、情緒影響和腹瀉。
|
| 交互作用 |
|
|
強效 CYP3A 抑制劑對 lorlatinib 的影響:併用itraconazole(強效 CYP3A 抑制劑)會使口服單劑量LORVIQUA 100 毫克的 AUCinf 升高 42%,Cmax 升高 24%。
Lorlatinib 對 CYP3A 受質的影響:連續15 日、每日一次口服LORVIQUA 150毫克會使口服單劑量midazolam(一種敏感的 CYP3A 受質)2 毫克的AUCinf 降低 64%,Cmax 降低50%。
|
| 禁忌 |
|
|
基於發生嚴重肝臟毒性的可能性,LORVIQUA 禁止使用於正在接受強效CYP3A 誘導劑的病人。
|
| 給付規定 |
|
9.81.Lorlatinib (如Lorviqua):(109/6/1、112/11/1、113/4/1)
1.適用於ALK陽性的晚期非小細胞肺癌第一線治療。(112/11/1)
(1)須經事前審查核准後使用:
I.每次申請事前審查之療程以三個月為限,每三個月需再次申請。
II.初次申請時需檢具確實患有非小細胞肺癌之病理或細胞檢查報告,以及符合本保險醫療服務給付項目及支付標準伴隨式診斷編號30105B規定之ALK突變檢測報告。
III.再次申請時並需附上治療後相關臨床資料,如給藥4週後,需追蹤胸部X光或電腦斷層等影像檢查評估療效,往後每4週做胸部X光檢查,每3個月需追蹤其作為評估藥效的影像(如胸部X光或電腦斷層),若病情惡化即不得再次申請。
(2)Lorlatinib與alectinib、ceritinib、crizotinib、brigatinib用於ALK陽性之晚期非小細胞肺癌第一線治療時,僅得擇一使用,除因病人使用後,發生嚴重不良反應或耐受不良之情形外,不得互換。
2.適用於在ceritinib、alectinib或brigatinib治療中惡化之ALK陽性的晚期非小細胞肺癌患者。(109/6/1、112/11/1、113/4/1)
(1)須經事前審查核准後使用。
(2)每次申請事前審查之療程以三個月為限,每三個月需再次申請,再次申請時並需附上治療後相關臨床資料,若病情惡化即不得再次申請。
|
| 注意事項 |
|
|
1. 若遺漏劑量時應補服,除非下個劑量的服藥時間在4小時以內。請勿為了補足漏服的劑量而同時服用2個劑量。 2. 若在服用LORVIQUA 後發生嘔吐,請勿服用額外劑量,但應繼續服用下個排定劑量。
|
| 警語 |
|
LORVIQUA 禁用於正在服用強效 CYP3A 誘導劑的病人。在開始服用
LORVIQUA 之前,停用強效 CYP3A 誘導劑,停用的時間相當於強效 CYP3A誘導劑的3 個血漿半衰期。
避免 LORVIQUA 與中效 CYP3A 誘導劑併用。如果不能避免併用中效 CYP3A誘導劑,則應在開始服用 LORVIQUA 後 48 小時監測 AST、ALT 和膽紅素(bilirubin),然後在開始服用 LORVIQUA 後第一週進行至少3 次監測。
對於持續 2 级或更嚴重肝毒性的病人,應根據每種藥物的相對重要性,停止使用LORVIQUA 或CYP3A 誘導劑。
|
| 藥品保存方式 |
|
|
請儲存於30ºC 以下。
|







































