| 結構式 |
|
|
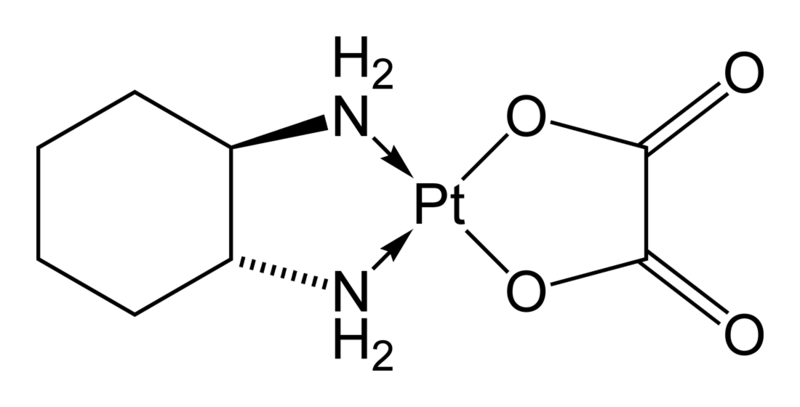
Oxaliplatin:
(R,R)-1,2-diaminocyclohexane(ethanedioate-O,O)platinum
|
| UpToDate |
UpToDate 連結
|
| 藥理作用 |
|
1. 本品為新一代platinum類之抗癌藥,其為oxalate和1,2-diaminocyclohexane("DACH")與platinum原子所組成之複合物。
2. Oxaliplatin 對於許多的腫瘤細胞模型系統包括人類結腸直腸癌模型,具極廣泛的體外細胞毒性及體內抗腫瘤活性。在許多已對 cisplatin 產生抗藥性的腫瘤細胞模型中,oxaliplatin 亦被證實具體外及體內活性。
3. Oxaliplatin 和 5-FU 併用時,體外和體內詴驗證實有細胞毒性加成作用。
4. Oxaliplatin 的作用機轉雖尚未完全明瞭,仍顯示其經生體轉化後之水解產物與去氧核糖核酸(DNA)作用後,形成 DNA 股內及股間的交互聯結(intra and interstrand crosslinks),經破壞 DNA 合成達到細胞毒性及抗癌效果。
|
| 適應症 |
|
和 5-fluorouracil(5-FU)及 folinic acid(FA)併用,作為
1.第三期結腸癌(Duke's C)原發腫瘤完全切除手術後的輔助療法。
2.治療轉移性結腸直腸癌 Oxaliplatin 和 Capecitabine 併用可用於局部晚期及復發/轉移性胃癌之治療。
|
| 用法用量 |
|
Oxaliplatin 使用於手術後輔助療法的建議劑量為 85mg/m2,以靜脈途徑給藥,每 2 週給藥一次,持續 12 個療程(6個月)。 Oxaliplatin 使用於治療轉移性結腸直腸癌的建議劑量為85mg/m2,以靜脈途徑給藥,每 2 週給藥一次。
Oxaliplatin 使用於治療局部晚期及復發性/轉移性胃癌的建議劑量為每 3 週 130mg/m2(在治療期的第一天及第八天給予 65 mg/m2),以靜脈途徑給藥。
劑量應依病人耐受性來調整。
當oxaliplatin 和 fluoropyrimidines 併用時,應在給與fluoropyrimidine前(例如 5-fluorouracil)先給與oxaliplatin。
Oxaliplatin 一般以 250~500ml 的 5%葡萄糖注射液(50mg/ml)稀釋至濃度介於 0.2 mg/ml 及 0.70 mg/ml 之間;而後以持續 2~6 小時點滴給藥。在臨床使用上,以 oxaliplatin 85 mg/m2的劑量投與時,0.70 mg/ml 為最高稀釋濃度。
通常 oxaliplatin 和 5-fluorouracil 併用,以靜脈點滴給藥。每兩週重複給藥一次的治療,其 5-FU 的給藥方式亦可以 bolus dose 合併靜脈點滴給藥。
用法
Oxaliplatin 以點滴給藥。
給予 oxaliplatin 時,病患不需要先給予過多的水分。
以 250~500ml 的 5%葡萄糖注射液稀釋成濃度不低於 0.2 mg/ml 的注射液後之 oxaliplatin 必須由中央靜脈管或週邊靜脈持續 2~6 小時點滴給藥。 Oxaliplatin 一定要在 5-FU 之前先輸注。
當發生藥物外滲時,應立即停藥。
藥品之處理
Oxaliplatin 在給藥前應先稀釋再靜脈點滴給藥,僅有 5%葡萄糖注射液才可以用來稀釋本藥。
|
| 藥動力學 |
|
|
Oxaliplatin 在體外的生體轉化作用不經酵素降解,亦無任何跡象顯示其 diaminocyclohexane cycle (DACH)經 cytochrome P450代謝。 Oxaliplatin 在體內受到廣泛的生體轉化作用,兩小時點滴給藥終止時,在超微濾血漿中無法偵測到未代謝原型,在全身循環中可偵測到許多細胞毒性代謝物包括 monochloro-,dichloro-和 diaquo-DACH platinum 型式者,並於稍後可偵測到一些無活性的接合產物。 Platinum 主要由尿液中排除,主要的清除率出現在投藥後 48 小時內。在第 5 天,約有 54%的總劑量經由尿液排除,小於 3%的總劑量經由糞便排除。
|
| 副作用 |
|
造血系統:貧血、白血球減少症、顆粒性血球減少症和血小板減少症;胃腸系統:噁心、嘔吐和腹瀉;神經系統:末梢感覺異常,常見的症狀有痙攣性疼痛、口部周圍、上呼吸道以及消化道感覺異常;其他的副作用:發燒、發紅,但未有脫髮或聽覺、肝腎或心臟的不良反應。
|
| 交互作用 |
|
|
應注意oxaliplatin治療併用已知會引起QT間期延長的其他藥品。若同時併用此類藥品組合,應密切監測QT間期。
|
| 禁忌 |
|
|
Oxaliplatin 禁用於下列病人:
1. 對 oxaliplatin 過敏者。
2. 授乳婦女
3. 治療前有骨髓抑制(myelosuppression)現象的病人(嗜中性白血球數目< 2 x 109 /L 或血小板數目< 100 x 109 /L )
4. 治療前有周邊感覺神經病變且功能異常者
5. 重度腎功能不良的病人(creatinine clearance<30ml/min)
|
| 給付規定 |
|
9.10.Oxaliplatin:(需符合藥品許可證登載之適應症)(89/7/1、91/10/1、93/8/1、98/2/1、98/3/1、98/7/1、102/9/1、102/12/1、109/12/1、110/5/1、110/6/1、110/7/1、111/11/1、113/4/1)
1.和5-FU和folinic acid併用
(1)治療轉移性結腸直腸癌,惟若再加用irinotecan (如Campto)則不予給付。(91/10/1)
(2)作為第三期結腸癌(Duke`s C) 原發腫瘤完全切除手術後的輔助療法。(98/2/1)
2.與fluoropyrimidine類藥物(如capecitabine、5-FU、UFUR,但不包含TS-1)併用,可用於局部晚期及復發/轉移性胃癌之治療。(須依藥品許可證登載之適應症使用)。(98/2/1、98/3/1、98/7/1、102/9/1、102/12/1、109/12/1)
3.與5-fluorouracil、leucovorin及irinotecan併用(FOLFIRINOX),作為轉移性胰臟癌之第一線治療。(110/5/1、110/6/1、110/7/1、111/11/1)
4.與nivolumab 120mg及 fluoropyrimidine(5-FU或capecitabine)併用於第一線治療晚期或轉移性且不具有HER2過度表現的胃癌病人,病人需符合免疫檢查點抑制劑之藥品給付規定。(113/4/1)
|
| 注意事項 |
|
Oxaliplatin 僅可在具有給予抗癌藥物設備之醫療機構使用,oxaliplatin 應在有經驗的臨床腫瘤醫師的監督下使用。
由於重度腎功能不良的病人的安全性資料有限,用藥前應先評估其利弊。曾對其他platinum類藥物過敏的病患使用oxaliplatin時應密切監測其過敏反應,過敏反應有可能在任何治療週期發生。若有疑似對 oxaliplatin 過敏的反應發生時,應立即停藥,且開始採取合適的症狀治療,對於此類病人禁止再次使用 oxaliplatin。若有 oxaliplatin 外滲的情況發生時,應立即停止點滴給藥且開始採取合適的方法治療局部症狀。使用 oxaliplatin 時應小心監測其神經毒性,尤其是和其他有特殊神經毒性的藥品併用時,應在每次給藥前進行神經學檢查,之後亦應做定期的神經學檢查。
|
| 過量處理 |
|
|
目前 oxaliplatin 尚無解毒劑,過量時其不良反應會加劇,此時應開始監測血液學參數並針對症狀給予治療。
|
| 藥品保存方式 |
|
本品以 5% glucose 稀釋後,其使用中的化學及物理安定性為:在 2℃到 8℃ 下可保存 48 小時,在 25℃下可保存 24 小時。
以微生物觀點而言,輸注溶液應立即使用。如不立即使用,使用者要自行判斷經稀釋後於使用前的狀況和效期,在 2℃到 8℃的溫度下不應超過 24 小時,除非稀釋過程是在無菌和確效的情況下操作的。
【儲 存】 :25℃以下儲存。
|







































