| 結構式 |
|
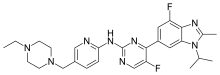
Abemaciclib
2-Pyrimidinamine, N-[5-[(4-ethyl-1-piperazinyl) methyl]-2-pyridinyl]-5-fluoro-4-[4-fluoro-2-methyl-1-(1-methylethyl)-1H-benzimidazol-6-yl]-。
|
| UpToDate |
UpToDate 連結
|
| 藥理作用 |
|
|
Abemaciclib是細胞週期蛋白依賴性激酶4和6 (CDK4和CDK6)的抑制劑。這些激酶在與D細胞週期蛋白(D-cyclins)結合後被活化。在雌激素受體陽性(ER+)的乳癌細胞株中,細胞週期蛋白D1和CDK4/6促進視網膜母細胞瘤蛋白(Rb)的磷酸化、細胞週期進展和細胞增生。在體外試驗中,連續暴露於abemaciclib抑制了Rb磷酸化並阻斷從細胞週期的G1期進入S期,導致細胞衰老和細胞凋亡。在乳癌異種移植模型中,每日不間斷單獨給予abemaciclib或併用抗雌激素藥物,均導致腫瘤尺寸縮小。
|
| 適應症 |
|
1. 早期乳癌:
併用內分泌療法 (tamoxifen或芳香環酶抑制劑 ),可做為荷爾蒙受體(HR)陽性、第二型人類表皮生長因子受體(HER2)陰性、淋巴結陽性,高復發風險之早期乳癌成年病人的輔助治療。
2. 晚期乳癌:
(1) 併用芳香環酶抑制劑(aromatase inhibitor),可做為治療荷爾蒙受體(HR)陽性、第二型人類表皮生長因子受體(HER2)陰性之晚期或轉移性乳癌之停經後婦女及男性的第一線內分泌療法(endocrine-based therapy)。
(2) 併用fulvestrant,可治療荷爾蒙受體(HR)陽性、第二型人類表皮生長因子受體(HER2)陰性,且接受內分泌療法後疾病惡化之晚期或轉移性乳癌的成人病人。
(3) 單獨用於治療荷爾蒙受體(HR)陽性、第二型人類表皮生長因子受體(HER2)陰性,曾經接受過內分泌治療及於轉移後接受化學治療後又發生疾病惡化之晚期或轉移性乳癌的成人病人。
|
| 用法用量 |
|
1. 與fulvestrant, 內分泌療法(tamoxifen或芳香環酶抑制劑)併用時,VERZENIO的建議劑量為150 mg,每日口服兩次。關於fulvestrant, tamoxifen或芳香環酶抑制劑的建議劑量,請參閱其完整的處方資訊。 2. 接受VERZENIO 與芳香環酶抑制劑合併治療的停經前/停經前後(pre/perimenopausal)的婦女及男性,應依據目前的臨床實務標準接受促性腺激素釋放激素致效劑(gonadotropin-releasing hormone agonist, GnRH)治療。
3. 接受VERZENIO 與fulvestrant合併治療的停經前/停經前後(pre/perimenopausal)的婦女,應依據目前的臨床實務標準接受促性腺激素釋放激素致效劑(GnRH)治療。
4. 單獨使用時,VERZENIO的建議劑量為200 mg,每日口服兩次。
5. 對於早期乳癌(EBC),持續使用VERZENIO,直到2年治療結束或直到疾病復發或出現無法耐受的毒性。
6. 對於晚期或轉移性乳癌(MBC),持續治療直到疾病惡化或出現無法耐受的毒性。
7. VERZENIO可隨餐或空腹使用。
8. 指示病人每天於大約相同的時間服用VERZENIO。
9. 如果病人服用VERZENIO後嘔吐或漏服一劑藥物,請病人依照排定時間服用下一劑藥物。病人應吞服整顆VERZENIO錠劑,不可將錠劑咀嚼、壓碎或切半後吞服。
10. VERZENIO錠劑如果破裂、裂開或不完整,請病人不要服用。
|
| 藥動力學 |
|
藥物吸收
給予單次口服劑量200 mg,abemaciclib的絕對生體可用率為45% (19% CV)。Abemaciclib的Tmax中位數為8.0小時(範圍:4.1至24.0小時)。
分佈
體外試驗顯示,於濃度範圍152 ng/mL至5066 ng/mL,abemaciclib與人類血漿蛋白、血清白蛋白及α-1-酸性糖蛋白的結合,不受濃度影響。在一項臨床試驗中,abemaciclib的結合率平均值(標準差,SD)為96.3% (1.1)、M2為93.4% (1.3)、M18為96.8% (0.8),而M20為97.8% (0.6)。全身分佈體積幾何平均值約為690.3 L (49% CV)。
晚期癌症(包括乳癌)病人,其腦脊髓液中abemaciclib及其活性代謝產物M2和M20的濃度與非結合的血漿濃度相當。
排除
病人的abemaciclib肝臟清除率(CL)幾何平均值為26.0 L/h (51% CV),而病人的abemaciclib血漿清除半衰期平均值為18.3小時(72% CV)。
代謝
肝臟代謝為abemaciclib清除的主要途徑。Abemaciclib主要透過P450 (CYP) 3A4代謝成多種代謝產物,N-desethylabemaciclib (M2)的形成代表主要代謝路徑。其他代謝產物包括hydroxyabemaciclib (M20)、hydroxy-N-desethylabemaciclib (M18),及一種氧化代謝產物(M1)。M2、M18和M20的效力與abemaciclib相當,且其AUC分別佔血漿中總循環分析物的25%、13%和26%。
排泄
單次投予放射性標定abemaciclib口服劑量150 mg後,約81%的劑量自糞便回收,3%的劑量自尿液回收。糞便排除的劑量大多為代謝產物。
|
| 副作用 |
|
|
最常見之不良反應包括腹瀉、感染、嗜中性球低下症、貧血、疲倦、噁心、嘔吐和食慾不振。
|
| 交互作用 |
|
強效CYP3A抑制劑:Ketoconazole (強效CYP3A抑制劑)預計會使abemaciclib的AUC增加最高達16倍。
中效CYP3A抑制劑: Verapamil 及diltiazem(中效CYP3A抑制劑)預計分別會使abemaciclib及其活性代謝產物(M2、M18與M20)經相對效力調整之非結合AUC增加約1.6倍和2.4倍。
強效CYP3A誘導劑:健康受試者併用rifampin(強效CYP3A誘導劑)600 mg的每日劑量及VERZENIO單次200 mg,使abemaciclib及其活性代謝產物(M2、M18與M20)經相對效力調整之非結合AUC0-INF降低約70%。
中效CYP3A誘導劑:Efavirenz、bosentan和modafinil(中效CYP3A誘導劑)預期使abemaciclib及其活性代謝產物(M2、M18與M20)經相對效力調整之非結合AUC分別降低53%, 41%及29%。
葡萄柚可能與VERZENIO產生交互作用。告知病人在接受VERZENIO治療期間,應避免食用葡萄柚製品。
|
| 禁忌 |
|
|
對於VERZENIO內之有效成份或賦形劑過敏者。
|
| 給付規定 |
|
9.107.Abemaciclib (如Verzenio):(113/3/1)
1.併用內分泌療法,作為荷爾蒙受體(HR)陽性(ER或PR>30%)、第二型人類表皮生長因子受體(HER2)陰性、淋巴結陽性,高復發風險之早期乳癌成年女性病人的輔助療法,須符合下列高復發風險條件之一:
(1)pALN (positive axillary lymph nodes,陽性腋下淋巴結)≥ 4。
(2)pALN (陽性腋下淋巴結)為1-3 且腫瘤大小≥ 5 cm。
(3)pALN (陽性腋下淋巴結)為1-3 且腫瘤細胞分化第3級。
2.使用前,須接受標準之化學及放射輔助治療方可申請使用。使用中,若疾病惡化須停止使用且不得再使用其他CDK4/6抑制劑。
3.使用前,僅能接受最多12週的內分泌治療,且應於手術切除後16個月內接受本品治療。
4.須經事前審查核准後使用,每24週須再次申請並檢附療效評估資料,若疾病有惡化情形須停止使用。
5.每日至多使用2錠,使用不得超過2年。
|
| 注意事項 |
|
腹瀉
可能導致腹瀉,在某些案例中可能較為嚴重。
• 早期發現及介入治療對於能否適當處置腹瀉極為重要。指示病人一旦發現有稀便的情況,即應開始止瀉劑治療(例如loperamide),並通知其醫療照護人員以利提供進一步指示及適當追蹤。
• 建議病人增加口服液體攝取量。
• 經由止瀉療法治療後,若腹瀉未於24小時內緩解至≤第1級,則暫停Verzenio給藥。靜脈血栓栓塞告知病人若有任何血栓栓塞的徵兆或症狀,例如肢體疼痛或腫脹、呼吸短促、胸痛、呼吸急促和心跳過快等,應立即聯絡其醫療照護人員。
ERZENIO對操作機械和駕駛交通工具會有輕微影響。疲倦和頭暈為VERZENIO 非常常見之不良反應,需告知病人於疲倦或頭暈時操作機械和駕駛交通工具須小心。
|
| 藥品保存方式 |
|
|
儲存於 30°C 以下。
|







































